
| A. | BrCl的化学性质和Cl2相似,Cl2与水反应是氧化还原反应,BrCl+H2O=HCl+HBrO也是氧化还原反应 | |
| B. | 弱碱性条件下,甲酸乙酯能与氢氧化铜反应,乙酸乙酯也能与氢氧化铜反应 | |
| C. | 苯不能使酸性高锰酸钾褪色,甲苯也不能使酸性高锰酸钾褪色 | |
| D. | CO2与SiO2均为酸性氧化物,CO2能与NaOH溶液反应,SiO2也能与NaOH溶液反应 |
分析 A.根据元素的化合价的变化分析;
B.乙酸乙酯与氢氧化铜不反应;
C.甲苯与高锰酸钾发生氧化还原反应;
D.CO2与SiO2均为酸性氧化物,都可与碱反应生成盐和水.
解答 解:A.BrCl+H2O=HCl+HBrO中元素的化合价没有发生变化,不是氧化还原反应,故A错误;
B.甲酸乙酯含有醛基,能与氢氧化铜发生氧化反应,而乙酸乙酯与氢氧化铜不反应,故B错误;
C.甲苯与高锰酸钾发生氧化还原反应,被氧化为苯甲酸,而苯与酸性高锰酸钾不反应,故C错误;
D.CO2与SiO2均为酸性氧化物,都可与碱反应生成盐和水,故D正确.
故选D.
点评 本题考查化学反应原理的探究,为高频考点,侧重于学生的分析能力的考查,注意物质性质的异同,不能一概而论,注意把握反应的机理,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32 g O3含有的氧原子数目为2NA | |
| B. | 5.6 g的Fe在足量Cl2中完全燃烧转移电子数为0.2NA | |
| C. | 0.1 mol•L-1 Na2SO4溶液含有的钠离子数目为0.2NA | |
| D. | 标准状况下,22.4 L苯含有的碳原子数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
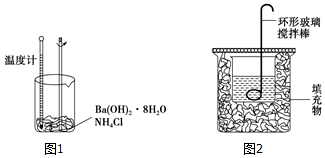
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com