
短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的是
A. Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应
B. 原子半径Z>W>Y>X
C. 气态氢化物的稳定性Z>W
D. X的气态氢化物与足量W单质在光照条件下反应生成物均为气体
【知识点】元素周期表、元素周期律的应用
【答案解析】A 解析:X与Z同主族,并且原子序数之和为20,X是碳元素,Z是硅元素;Y原子的质子数为Z原子的质子数的一半,Y 是氮元素;W原子的最外层电子数比Y原子的最外层电子数多2个,W是氯元素;A、Y的最高价氧化物对应的水化物是硝酸,可与其气态氢化物氨气发生化合反应,故A正确;B、同周期从左到右半径减小,同主族从上到下半径增大,故原子半径Z>W> X > Y,故B错误;C、非金属性判据之一是氢化物的稳定性,非金属性W>Z, 气态氢化物的稳定性W>Z,故C错误;D、X的气态氢化物甲烷与足量W单质氯气在光照条件下反应生成物一氯甲烷为气体,其余有机产物为液体,故D错误。
故答案选A
【思路点拨】本题考查了元素周期律的应用,涉及元素周期律、原子半径比较、气态氢化物的稳定性等,判断元素是解题关键,难度不大。


科目:高中化学 来源: 题型:
可逆反应:2NO2 2NO+O2 在密闭容器中反应,达到平衡状态的标志是:( )
2NO+O2 在密闭容器中反应,达到平衡状态的标志是:( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2 的同时,生成2n mol NO
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
A. ①④⑥ B.②③⑤ C.①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钠俗称红矾钠(Na2Cr2O7·2H2O),是重要的化工产品和强氧化剂。工业制备红矾钠的流程如下:

(1)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成 。
(2)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:4Fe(CrO2)2+8Na2CO3+7O2 = 2Fe2O3+8Na2CrO4+8CO2 。为了加快该反应的反应速率,可采取的措施是 。(写一种即可)
(3)已知CrO42-在不同的酸性溶液中有不同的反应,如:
2CrO42-+2H+= Cr2O72-+H2O; 3CrO42-+4H+= Cr3O102-+2H2O
① 往混合溶液甲中加入硫酸必须适量的原因是 。
② 混合溶液乙中溶质的化学式是 。
(4)在含Cr2O72-废水中存在着平衡:Cr2O72-+H2O 2CrO42-+2H+,请写出该平衡的平衡常数表达式K= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式K= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
(5)请配平碱性溶液还原法中发生的离子反应:
□Cr2O72-+□S2-+□H2O ——□Cr(OH)3+□S2O32-+□OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示:
(1)“焙烧”过程中Al2(SO4)3和S发生反应的化学方程式为 ;
若生成102g Al2O3,转移的电子数目为 ;
(2)生成沉淀Ⅰ时的离子方程式为 ;
(3)写出化学式:沉淀Ⅱ是 ;
(4)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀Ⅰ,证明沉淀Ⅰ已洗涤干净的实验操作和现象是 ;
(5)从滤液中得到K2SO4晶体的方法是 ;
(6)K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E均为中学化学常见物质,A是短周期原子半径最大的元素(稀有气体除外)构成的单质,E既可溶于盐酸又可溶于NaOH溶液,它们之间的反应关系如图所示:
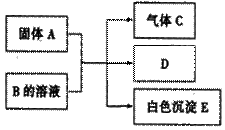
(1)E溶于NaOH溶液的离子方程式为 ;
(2)工业上冶炼A的化学反应方程式为 ;
(3)气体C在使用前需要检验纯度,操作方法
是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫铁矿烧渣的主要成分为Fe2O3、Fe3O4,以及少量SiO2、Al2O3等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:

已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号) 。
(2)Fe粉除调pH外,另一个作用是 ;Fe粉调节溶液的pH为 。
(3)“沉淀、过滤”步骤中生成FeCO3的离子方程式为 ;
所得滤液的主要溶质是(填化学式) 。
(4)高温条件下,“氧化”步骤中发生反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com