
| A. | Na2CO3 | B. | AgNO3 | C. | NaHCO3 | D. | 酚酞 |
分析 CH3COOH、Ba(OH)2、Al2(SO4)3、CaCl2分别与NaHCO3反应的现象为:气体生成、白色沉淀、白色沉淀和无色气体、无现象,以此来解答.
解答 解:A.Ba(OH)2、CaCl2均与碳酸钠反应生成白色沉淀,不能鉴别,故A不选;
B.Al2(SO4)3、CaCl2均与硝酸银反应生成白色沉淀,不能鉴别,故B不选;
C.CH3COOH、Ba(OH)2、Al2(SO4)3、CaCl2分别与NaHCO3反应的现象为:气体生成、白色沉淀、白色沉淀和无色气体、无现象,现象不同,可鉴别,故C选;
D.CH3COOH、Al2(SO4)3、CaCl2均遇酚酞为无色,不能鉴别,故D不选;
故选C.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应及反应现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 滴加稀盐酸 | 有气泡产生 | 原溶液中有CO32- |
| B | 滴加盐酸酸化的 BaCl2溶液 | 生成白色沉淀 | 原溶液中有Ag+ 或SO42- |
| C | 用洁净铂丝蘸取溶液 进行灼烧 | 火焰呈黄色 | 原溶液中有Na+、 无K+ |
| D | 滴加稀NaOH溶液,将湿 润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

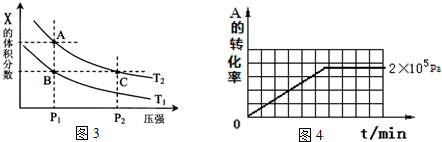
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和澄清石灰水 | B. | NaOH溶液和CO2 | ||
| C. | Na2CO3溶液和盐酸 | D. | NaHCO3溶液和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
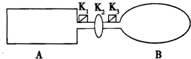 如图装置中,A是由导热材料制成的密闭容器,B是耐化学腐蚀且易于传热的透明气球,关闭K2,将等量的1molNO2通过K1、K3分别充A、B中,反应起始时,A、B的体积相同均为a L.已知:2NO2(g)?N2O4(g)△H<0
如图装置中,A是由导热材料制成的密闭容器,B是耐化学腐蚀且易于传热的透明气球,关闭K2,将等量的1molNO2通过K1、K3分别充A、B中,反应起始时,A、B的体积相同均为a L.已知:2NO2(g)?N2O4(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na 着火可以使用泡沫灭火器 | |
| B. | 绿色化学是指有毒气体尾气要经过无毒处理后在排放 | |
| C. | 实验室用浓硫酸溶解铜制备硫酸铜 | |
| D. | 实验室可以适当温度下,使铜片在持续通入空气的稀硫酸中溶解的方法制备硫酸铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com