
| A.固体CH3COOK | B.固体CH3COONH4 | C.NH3气体 | D.固体NaHCO3 |
 CH3COO-+H+,CH3COO-+H2O
CH3COO-+H+,CH3COO-+H2O CH3COOH+OH-。醋酸溶液中加入醋酸钠晶体,溶液的pH虽然增大,但只会小于7。因此CH3COOH的电离平衡占主导地位,乙同学的解释正确。为了验证两种解释哪种正确,就得选择一种含有CH3COO-但水解不显碱性的物质再实验,它只能是CH3COONH4。
CH3COOH+OH-。醋酸溶液中加入醋酸钠晶体,溶液的pH虽然增大,但只会小于7。因此CH3COOH的电离平衡占主导地位,乙同学的解释正确。为了验证两种解释哪种正确,就得选择一种含有CH3COO-但水解不显碱性的物质再实验,它只能是CH3COONH4。 CH3COO-+H+,H2O=====H++OH-。因此,溶液中存在Na+、Cl-、CH3COOH、CH3COO-、H2O、H+、OH-等7种粒子。根据物料守恒,n(CH3COOH)+n(CH3COO-)=n(Na+)=0.010mol,根据电荷守恒,n(CH3COO-)+c(OH-)+c(Cl)-=n(Na+)+n(H+),因此,n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol。
CH3COO-+H+,H2O=====H++OH-。因此,溶液中存在Na+、Cl-、CH3COOH、CH3COO-、H2O、H+、OH-等7种粒子。根据物料守恒,n(CH3COOH)+n(CH3COO-)=n(Na+)=0.010mol,根据电荷守恒,n(CH3COO-)+c(OH-)+c(Cl)-=n(Na+)+n(H+),因此,n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol。

科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若pH>7时,则一定是c1v1=c2v2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,可能有c1/c2 > v2/v1 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+C(CH3COOH)=C(Na+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol/L氨水中c(NH4+)=c(OH-) |
| B.等体积等物质的量浓度的CH3COOH和NaOH溶液混合后 c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.pH=2的HA溶液和pH=12的MOH溶液以任意比混合的溶液中 c(H+)+c(M+)=c(OH-)+C(A-) |
| D.常温下,pH=7的氯化铵与氨水的混合溶液中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.c(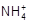 )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) | B.c(Cl-)>c(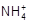 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
C.c(Cl-)>c(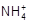 )>c(H+)>c(OH-) )>c(H+)>c(OH-) | D.c(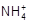 )+c(H+)=c(Cl-)+c(OH-) )+c(H+)=c(Cl-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3COOH+OH-,下列说法正确的是
CH3COOH+OH-,下列说法正确的是| A.加入少量NaOH固体,c(CH3COO-)减小 |
| B.加入少量FeCl3固体,c(CH3COO-)减小 |
| C.稀释溶液,溶液的pH增大 |
| D.加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| C.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-) | D.c(OH-)=c(H+)+c(H2CO3)+c(HCO3-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com