
| A. | 乙烯聚合为聚乙烯高分子材料符合绿色化学原子经济性要求 | |
| B. | 银制品久置干燥空气中因电化学腐蚀而使表面变暗 | |
| C. | 重金属盐能使蛋白质变性,所以误食重金属盐会中毒 | |
| D. | 在合成洗涤剂中添加酶制剂可以提高洗涤效果 |
分析 A、绿色化学又称“环境无害化学”,核心就是要利用化学原理从源头消除污染;
B、银能和空气中氧气反应使表面变暗;
C、重金属盐能使蛋白质变性;
D、添加酶制剂可除去某些特殊的污渍;
解答 解:A、乙烯聚合为聚乙烯高分子材料,发生聚合反应,原子利用率为100%,符合绿色化学的核心意义,故A正确;
B、纯银饰品长久置表面变暗是由于金属银和空气中的氧气发生反应生成氧化银的结果,属于化学腐蚀,与电化学腐蚀无关,故B错误;
C、重金属盐能使蛋白质变性,所以误食重金属盐会中毒,喝豆浆或生鸡蛋可以解毒,故C正确;
D、合成洗涤剂中添加酶制剂可除去某些特殊的污渍,如血渍、汗渍,提高洗涤效果,故D正确;故选B.
点评 本题考查合成洗涤剂的原理,题目难度不大,注意在洗涤剂烷基苯磺酸钠中,烷基应以直链为宜,因为支链很难被细菌降解而使水体污染,为易错点.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
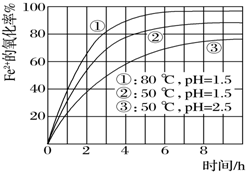 为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,判断下列说法错误的是( )
为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,判断下列说法错误的是( )| A. | pH越小氧化率越小 | |
| B. | 温度越高氧化率越大 | |
| C. | Fe2+的氧化率除受pH、温度影响外,还受其它因素影响,如浓度等 | |
| D. | 实验说明降低pH、升高温度有利于提高Fe2+的氧化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时反应逆向进行 | |
| C. | 25℃时,反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数是0.5 | |
| D. | 恒温恒容,向已达平衡的容器中再充入少量Ni(CO)4(g),达到新平衡时,CO的体积百分含量将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 有机物 | 试剂 | 现象 |
| ①淀粉 ②苯乙烯 ③苯酚 ④蛋白质 | a.浓硝酸 b.酸性高锰酸钾溶液 c.碘水 d.FeCl3溶液 | A.呈紫色 B.呈蓝色 C.紫色褪去 D.呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
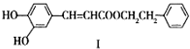 不饱和酯类化合物在药物、涂料等方面应用广泛.
不饱和酯类化合物在药物、涂料等方面应用广泛. .
.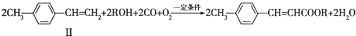
 (写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.
(写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.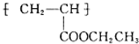 可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.
可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )| A. | 聚异丁烯可以通过加聚反应制得 | |
| B. | 聚异丁烯的分子式为(C4H8)n | |
| C. | 聚异丁烯能使溴的四氯化碳溶液褪色 | |
| D. | 聚异丁烯完全燃烧生成CO2 和H2O的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com