
下列关于化学键的说法中不正确的是( )
A.化学键可以使离子相结合,也可以使原子相结合
B.非金属元素的原子之间只能形成共价键
C.化学反应过程中,反应物分子内的化学键断裂,产物分子中化学键形成
D、化学键是一种作用力
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:填空题
写出下列反应的化学方程式
(1)制备乙酸乙酯 ;
(2)实验室制作硝基苯 ;
(3)乙醇的催化氧化 ;
(4)铝热法炼铁反应 ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素叙述正确的是
A.气态氢化物的稳定性:D>C B.原子半径:B>A>C>D
C.单质的还原性:B>A D.原子序数:b>a>c>d
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
对10mL1mol/L的盐酸与一小块大理石的化学反应CaCO3+2HCl=CaCl2+CO2↑+H2O,下列措施能使化学反应速率提高的是( )
A.加入一定量的CaCl2 B.加入5mL1.5mol/L的盐酸
C.加入15mL0.5mol/L的盐酸 D.加入5mLH2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+4OH—4e-=4H2O O2+2H2O+4e-=4OH- 据此作出判断,下列说法中错误的是( )
A.供电时的总反应是:2H2+O2=2H2O
B.产物为无污染的水,属于环境友好电池
C.燃料电池的能量转化率无法达到100%
D.H2在负极发生还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
下列递变规律正确的是( )
A.O、S、Na、K的原子半径依次增大
B.Na、Mg、Al、Si的还原性逐渐增强
C.HF、HCl、H2S、PH3的稳定性依次增强
D.KOH、Ca(OH)2、Mg(OH)2、Al(OH)3的碱性逐渐增强
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市等十校高三3月联考理综化学试卷(解析版) 题型:实验题
新型电池在飞速发展的信息技术中发挥着越来越重要的作用。Li2FeSiO4是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。其中一种制备Li2FeSiO4的方法为:
固相法:2Li2SiO3+FeSO4 Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2
某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:
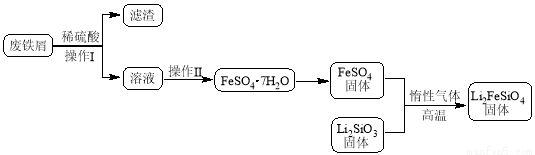
实验(二) Li2FeSiO4含量测定:

从仪器B中取20.00 mL溶液至锥形瓶中,另取0.2000 mol·Lˉ1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量。相关反应为:MnO4- +5Fe2++8H+=Mn2++5Fe3++4H2O,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积 | 20.00 mL | 19.98mL | 21.38mL | 20.02mL |
(1)实验(二)中的仪器名称:仪器B ,仪器C 。
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是 。
(3)操作Ⅱ的步骤 ,在操作Ⅰ时,所需用到的玻璃仪器中,除了普通漏斗、烧杯外,还需 。
(4)还原剂A可用SO2,写出该反应的离子方程式 ,此时后续处理的主要目的是 。
(5)滴定终点时现象为 ;根据滴定结果,可确定产品中Li2FeSiO4的质量分数为 ;若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的Li2FeSiO4含量 。(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第六次适应性考试理综化学试卷(解析版) 题型:选择题
在某温度时,将n mol·L-1氨水滴入10 mL 1.0 mol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
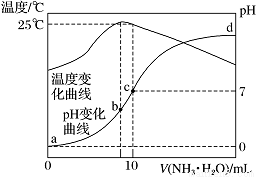
A.n=1.0
B.水的电离程度:b>c>a>d
C.c点:c(NH)=c(Cl-)=1.0 mol·L-1
D.25 ℃时,NH4Cl的水解常数(Kh)计算式为=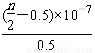
查看答案和解析>>
科目:高中化学 来源:2016届江西南昌二中、临川一中等高三4月联考二理综化学试卷(解析版) 题型:选择题
常温下,取pH=2的 HA溶液与HB溶液各1 mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示。下列叙述正确的是
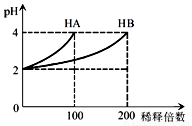
A.HA的电离方程式为HA H++A-
H++A-
B.稀释前,c(HB) > c(HA)=0.01 mol·L-1
C.0.1mol/L NaB溶液中: c(H+)= c(OH-)+c(HB)
D.NaA、NaB的混合溶液中:
2c(Na+)=c(A-)+c(B-)+c(HB)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com