
【题目】下列操作对应的现象和离子方程式均正确的是( )
操作 | 现象 | 离子方程式 | |
A | 饱和碳酸钠溶液中通入过量CO2 | 无明显变化 | CO |
B | 向苏打溶液溶液中滴加稀硫酸 | 立即产生气泡 | CO |
C | 向Ba(OH)2溶液中加足量NaHCO3溶液 | 生成白色沉淀 | 2HCO |
D | 向NaHCO3溶液中加入少量偏铝酸钠 | 生成白色沉淀和无色气体 | HCO |
A.AB.BC.CD.D
【答案】C
【解析】
A. 向饱和碳酸钠溶液中通入足量二氧化碳气体,有白色晶体析出,离子方程式:2Na++ CO![]() +CO2+H2O =2NaHCO3↓,故A错误;
+CO2+H2O =2NaHCO3↓,故A错误;
B. 向苏打溶液溶液中滴加稀硫酸,开始没有现象,后来产生气泡,离子方程式是: CO![]() +H+= HCO
+H+= HCO![]() ,HCO
,HCO![]() + H+= CO2↑+H2O,故B错误;
+ H+= CO2↑+H2O,故B错误;
C. 向Ba(OH)2溶液中加足量NaHCO3溶液,氢氧化钡少量,氢氧化钡电离出的钡离子和氢氧根离子完全反应,离子方程式是:2HCO![]() +Ba2++2OH-=BaCO3↓+2H2O+CO
+Ba2++2OH-=BaCO3↓+2H2O+CO![]() ,故C正确;
,故C正确;
D. 向NaHCO3溶液中加入少量偏铝酸钠,偏铝酸根离子促进碳酸氢根离子的电离,生成氢氧化铝白色沉淀和碳酸根离子,离子方程式是:HCO![]() +AlO
+AlO![]() +H2O=Al(OH)3↓+ CO
+H2O=Al(OH)3↓+ CO![]() ,故D错误;
,故D错误;
故选:C。


科目:高中化学 来源: 题型:
【题目】环戊二烯可用于制备二茂铁[Fe(C5H5)2];二茂铁分子是一种金属有机配合物,结构如图所示,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。下列说法正确的是( )
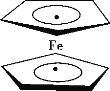
A.1mol环戊二烯(![]() )中含有5NA σ键
)中含有5NA σ键
B.二茂铁分子中存在配位键
C.环戊二烯分子中所有原子共平面
D.Fe2+的价电子排布式为3d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所得判断正确的是( )
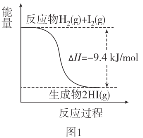
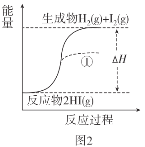
已知:I2(g)=I2(s) ΔH=-62.4kJ/mol
A.图1反应为吸热反应
B.图2反应的热化学方程式为2HI(g)![]() H2(g)+I2(g) ΔH=+9.4kJ/mol
H2(g)+I2(g) ΔH=+9.4kJ/mol
C.图2中若I2的状态为固态,则能量变化曲线可能为①
D.断裂1molH2(g)和1molI2(g)中化学键需要的能量大于断裂2molHI(g)中化学键需要的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用活性炭还原氮氧化物可防止空气污染。向1L密闭容器加入一定量的活性炭和NO,某温度下发生反应:
已知:①C(s)+2NO(g)![]() N2(g)+CO2 (g) ΔH
N2(g)+CO2 (g) ΔH
②C(s)+O2(g)![]() CO2 (g) ΔH1= -393.5 kJ/mol
CO2 (g) ΔH1= -393.5 kJ/mol
③N2(g)+O2(g)![]() 2NO(g) ΔH2= +180.5 kJ/mol
2NO(g) ΔH2= +180.5 kJ/mol
下列说法错误的是
A.ΔH= -574.0 kJ/mol
B.当容器内气体密度不变时,反应①达到平衡状态
C.反应③正反应的活化能大于180.5 kJ/mol
D.反应①达到平衡后,增大压强平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌是制造锌钡白和锌盐的主要原料,也可用作木材的防腐剂等。用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe2 O3、FeO等)生产ZnSO4·7H2O的流程如下:
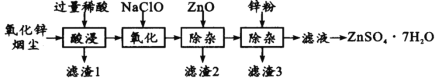
有关金属离子[c(Mn+)= 0.l mol/L]形成氢氧化物沉淀的pH范围如下表:
金属离 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 4.7 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 6.7 |
(1)“酸浸”时用的稀酸是____;滤渣1主要成分是____。
(2)“氧化”时的离子方程式为_________;加入ZnO除杂时溶液的pH控制范围是____~5.0。
(3)滤渣3含有锌和____;滤液得到ZnSO4·7H2O的操作是____、洗涤、干燥。
(4)取14.35gZnSO4·7H2O加热至不同温度,剩余固体的质量如下表
温度/℃ | 100 | 250 | 680 | 930 |
质量/g | 8. 95 | 8. 05 | 6. 72 | 4.05 |
则680℃时剩余固体的化学式为________(填序号)。
A.ZnO B.Zn3O(SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列说法中正确的是
A.室温下,盐酸中c(Cl-)与醋酸溶液中c(CH3COO-)相等,则两溶液的pH相等
B.将amol·L-1的醋酸溶液与0.01mol·L-1的氢氧化钠溶液等体积混合,溶液中:c(Na+)=c(CH3COO-),则醋酸的电离常数K=![]() (用含a的代数式表示)
(用含a的代数式表示)
C.向NH4Cl溶液中加入少量等物质的量浓度的稀盐酸,则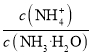 的值减小
的值减小
D.向Na[Al(OH)4]溶液中逐滴加入稀盐酸至沉淀恰好消失时:c(Cl-)=3c(Al3+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分是Cu2(OH)2CO3(含Fe2O3、FeCO3、Al2O3、SiO2杂质),工业上用孔雀石制备硫酸铜的第一步需用过量的硫酸溶解并过滤常温下,分别取滤液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
A.加入过量氨水:Fe3+、![]() 、
、![]() 、OH-
、OH-
B.加入过量NaOH溶液:Na+、[Al(OH)4]-、![]() 、OH-
、OH-
C.加入过量H2O2溶液:Fe2+、H+、![]() 、Cu2+
、Cu2+
D.加入过量 NaHCO3溶液:Na+、Al3+、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等且紧邻的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行1,2-二溴乙烷的消去反应,按下列步骤进行,请填空:

(1)按图连接好仪器装置并___。
(2)在试管a中加入2 mL 1,2-二溴乙烷和5 mL 10% NaOH的___溶液,再向试管中加入几片___。
(3)在试管b中加少量溴水。
(4)用水浴法加热试管里的混合物,持续加热一段时间后,把生成的气体通入溴水中,观察到的现象是____。
(5)①写出发生反应的化学方程式:__________。
②本实验中应注意的问题有______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com