

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 工业上利用Cl2和澄清石灰水反应来制取漂白粉 | |
| C. | 漂白粉的有效成分为Ca(ClO)2 | |
| D. | 除去与水反应的两个反应,图示其余转化反应均为氧化还原反应 |
分析 A.酸性氧化物是一类能与水作用生成酸或与碱作用生成盐和水或与碱性氧化物反应生成盐的氧化物;
B.工业上常用氯气和石灰乳反应来制取漂白粉;
C.根据漂白粉的成分分析;
D.凡是有化合价升降的反应都是氧化还原反应.
解答 解:A.CO不能与碱反应,不是酸性氧化物,故A错误;
B.澄清石灰水中氢氧化钙的浓度较小,氯气和石灰乳反应来制取漂白粉,故B错误;
C.氯气和石灰乳反应生成氯化钙和次氯酸钙,其中次氯酸钙具有强氧化性,则漂白粉的有效成分为Ca(ClO)2,故C正确;
D.除去与水反应,图示转化反应都是与氧气反应或氢气反应,都一定有化合价升降,均为氧化还原反应,故D正确.
故选CD.
点评 本题考查酸性氧化物、氧化还原反应、漂白粉的制取等,题目难度不大,注意澄清石灰水中氢氧化钙的浓度较小,应用石灰乳制取漂白粉.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.72 L Cl2与足量的水反应转移的电子数为0.3NA | |
| B. | 1 mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| C. | 常温常压下,4.6g NO2和N2O4混合物中含有的原子总数为0.3NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
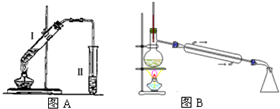
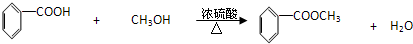 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯酸钾是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | 3mol氯气生成是有10摩尔电子转移 | |
| D. | 硫酸既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为10NA | |
| C. | 0.5 摩1,3-丁二烯分子中含有C=C双键数为 NA | |
| D. | 28g乙烯所含共用电子对数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温度同物质的量浓度时,HF比HCN易电离,NaF溶液的pH比NaCN溶液大 | |
| B. | 0.2 mol•L-1NH4Cl和0.1 mol•L-1 NaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O;c(NH4+)由大到小的顺序是:①>②>③>④ | |
| D. | 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 移去部分SO3 | B. | 增大容器容积 | C. | 降低体系温度 | D. | 通入大量O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com