
| A、熔融态的NaC1 | B、固体NaOH |
| C、铁 | D、稀硫酸 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、K+、Na+、HSO3-、NO3- |
| B、Na+、ClO-、SO42-、Cl- |
| C、NH4+、K+、SO42-、F- |
| D、Ag+、Na+、NO3-、CH3COOO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NaI的无色透明溶液:K+、Ba2+、OH-、MnO4- |
| B、1.2mol/L CaCl2溶液:NH4+、SO42-、Na+、NO3- |
| C、能使紫色石蕊试液变蓝色的溶液:Ba2+、NO3-、NH4+、SO32- |
| D、所含溶质为KHSO4的溶液:Fe2+、Mg2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)═c(H+) |
| C、0.1 mol?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、0.1 mol?L-1的硫化钠溶液中:c(OH-)=c(H+)>c(HS-)>c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性:FeCl3>Cl2>H2SO4>I2 |
| B、还原性:SO2>HI>FeCl2>HCl |
| C、2Fe+3I2=2FeI3 |
| D、6FeI2+3Cl2=2FeCl3+4FeI3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑦⑧ | B、①②⑥ |
| C、①⑤⑥⑧ | D、①④⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水与盐酸反应 |
| B、向醋酸溶液中加入适量NaOH溶液 |
| C、稀硫酸与Ba(OH)2溶液反应 |
| D、NaOH溶液与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④⑤ |
| C、①②④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
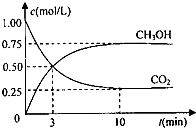 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com