
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | Z的最高价氧化物对应的水化物为弱酸 | |
| C. | 在一定条件下,与Y同主族的短周期元素某单质可以与氧化铁发生置换反应 | |
| D. | 常温下,0.1mol•L-1 W的氢化物水溶液的pH>1 |
分析 X、Y、Z、W均为短周期主族元素,原子序数依次递增.X与Z位于同一主族,Z的核外电子数是X的2倍,可知X为O,Z为S;Y、Z、W原子的最外层电子数之和等于Z的核外电子总数,设Y、W的最外层电子数为分别为x、y,W应为第三周期元素,则x+6+y=2+8+y,解得x=4,结合原子序数可知Y为Si,W只能为Cl,以此来解答.
解答 解:由上述分析可知,X为O,Y为Si,Z为S,W为Cl,
A.电子层越多,原子半径越大,同周期从左向右原子半径越小,则原子半径由小到大的顺序:X<W<Z<Y,故A错误;
B.Z的最高价氧化物对应的水化物为硫酸,属于强酸,故B错误;
C.在一定条件下,Y单质为Si,同主族元素C形成的单质高温下能与氧化铁发生置换反应,故C正确;
D.W的氢化物为HCl,常温下,0.1mol•L-1 W的氢化物水溶液的pH=1,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子结构为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 | |
| B. | p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多 | |
| C. | 某原子的电子排布式为1s22s2 2p63s2 3p63d54s1属于激发态 | |
| D. | Fe2+的电子排布式为1s22s2 2p63s2 3p63d6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学性质 | 实际应用 |
| A | 碳元素的非金属性比硅强 | 石英和碳粉的混合物高温下反应制备粗硅 |
| B | 乙醇能使蛋白质变性 | 无水乙醇作医用消毒机 |
| C | 明矾溶液显酸性 | 明矾作净水剂 |
| D | 油脂在碱性条件下水解 | 热的NaOH溶液鉴别植物油和矿物质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
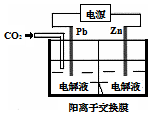 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Pb与电源的正极相连 | |
| B. | ZnC2O4在离子交换膜右侧生成 | |
| C. | 正极反应式为:Zn-2e-═Zn2+ | |
| D. | 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
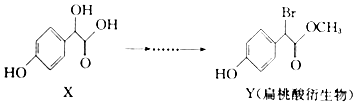
| A. | 化合物X的分子式为C8H8O4 | |
| B. | 化合物X、Y均可与NaHCO3溶液反应生成CO2 | |
| C. | 化合物X、Y分子中均含有1个手性碳原子 | |
| D. | 在一定条件下,化合物Y可发生加成反应和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
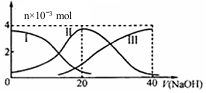 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )| A. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+3c(H2A)+c(HA-)=c(A2-)+2c(OH-) | |
| D. | 向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应一段时间后,X与Y的物质的量之比仍为1:1 | |
| B. | 达到平衡时,且反应放出0.1aKJ的热量 | |
| C. | 达到平衡后,若向平衡体系中充入稀有气体,Z的正反应速率将不发生变化 | |
| D. | X的体积分数保持不变,说明反应已达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 应用 | 解释 |
| A | 在相同条件下,在两支试管中各加入2mL 5% H2O2溶液,再向H2O2溶液中分别滴入1mL H2O和1mL 0.1mol•L-1 FeCl3溶液,对比观察现象 | 可以探究催化剂FeCl3对H2O2 分解速率的影响 |
| B | 向盛有1mL 0.01mol•L-1 AgNO3溶液的试管中滴加5滴0.01mol•L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01mol•L-1 KI溶液,产生黄色沉淀. | 常温下,Ksp(AgCl)>Ksp(AgI) |
| C | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出 | 蛋白质均发生变性 |
| D | 保存硫酸亚铁溶液需加入少量稀盐酸和铁钉 | 防止 Fe2+水解以及被 O2 氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com