
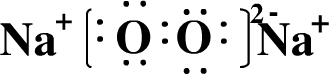 .
. .
. 分析 A、B、C、D四种短周期元素,气体A2与气体C2按体积比2:1混和后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体,该液体应为水,则可推知A为H,C为O,C、D同周期,D能形成自然界硬度最大的单质,则D为C,A、B同主族,B的阳离子与C的阴离子的核外电子排布相同,则B为Na,据此答题.
解答 解:A、B、C、D四种短周期元素,气体A2与气体C2按体积比2:1混和后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体,该液体应为水,则可推知A为H,C为O,C、D同周期,D能形成自然界硬度最大的单质,则D为C,A、B同主族,B的阳离子与C的阴离子的核外电子排布相同,则B为Na,
(1)根据上面的分析可知,A为氢元素,B为氧元素,C为氧元素,D为C,在周期表中的位置是第二周期第ⅣA族,故答案为:H;Na;O;第二周期第ⅣA族;
(2)B2C2为Na2O2,是离子化合物,其电子式为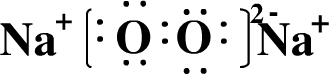 ,故答案为:
,故答案为: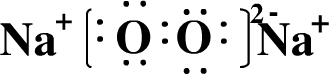 ;
;
(3)Na2O2和H2O生成NaOH和O2,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(4)H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ,故答案为:
,故答案为: .
.
点评 本题考查位置、结构、性质的关系及应用,为高频考点,元素的推断为解答的关键,侧重分析、推断能力的考查,题目难度不大.


 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:解答题
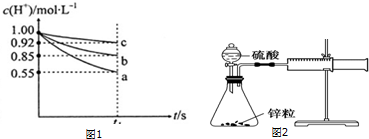
| 序号 | 加入的稀硫酸浓度 | 反应时间/min | 收集的气体/mL | 反应速率mL•min-1 |
| ① | 1mol•L-1 | 11 | 10 | |
| ② | 2mol•L-1 | a | 10 | b |
| ③ | 4mol•L-1 | 10 | 5.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
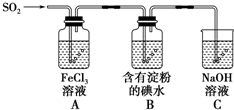 某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示
某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示查看答案和解析>>
科目:高中化学 来源: 题型:解答题
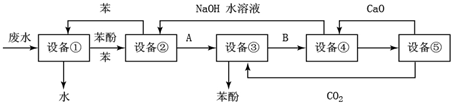 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
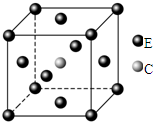 原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题:
原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na>Mg>Al | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4 | D. | 熔点:NaCl>H2O>CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com