
����Ŀ��������CH3COOH ��HCl ��H2SO4������Һ������Ҫ��ش��������⣺
��1��������pH��ͬʱ�������ʵ���Ũ�������� (�����)
��2�������ǵ����ʵ���Ũ����ͬʱ����pH��С�� (�����)
��3����c(H+)��ͬ�����������ˮϡ����ԭ����10����c(H+)�ɴ�С��˳��Ϊ (�����)��
��4����������ʵ���Ũ�Ⱦ���ͬ���٢ڢ���������Һ���ֱ�����ͬŨ�ȵ��ռ���Һǡ����ȫ��Ӧ�������ռ�������Ϊ ����ʱ���õ���������Һ��pH��С��ϵΪ ��
��5��������FeCl2��Һ��c(Fe2+)=2.0��10-2mol��L-1, c(Fe3��)=1.0��10-3mol��L-1, c(��)=5.3��10-2mol��L-1,�����Һ��PHԼΪ ��
��6��FeCl3������ˮ������ˮԭ���� (�����ӷ���ʽ����)��FeCl3��Һ�е�����Ũ�ȴӴ�С˳����
���𰸡�
��1��������2��������3����>��=����
��4��1:1:2����>��=������5��2��
��6��Fe3++3H2O![]() FeOH)3(����)+3H+��c(Cl-)>c(Fe3+)>c(H+)>c(OH-)��
FeOH)3(����)+3H+��c(Cl-)>c(Fe3+)>c(H+)>c(OH-)��
��������
�����������1��������pH��ͬʱ����Һ��������Ũ����ͬ�������ṩ1mol/L�������ӣ���Ҫ����Ũ��Ӧ����1mol/L����Ҫ��HCl��ҺŨ��Ϊ1mol/L����Ҫ��H2SO4 ��ҺŨ��Ϊ0.5mol/L�������ʵ���Ũ������Ϊ�����ʴ�Ϊ������
��2�������ǵ����ʵ���Ũ����ͬʱ������Ũ�ȶ���1mol/L����CH3COOH��Һ�����������Ũ��С��1mol/L����HCl�����������Ũ��Ϊ1mol/L����H2SO4�������������Ũ��Ϊ2mol/L��������Ũ��Խ����Һ��pHԽС������Һ��pH��С��Ϊ�����ʴ�Ϊ������
��3��������������ʼ�ˮϡ�ʹٽ����룬����ϡ�ͺ����������Ũ�������������������ӵ�Ũ��ֻ��С����ȣ�����c(H+)�ɴ�С��˳��Ϊ��������=�����ʴ�Ϊ��������=����
��4����������ʵ���Ũ�Ⱦ���ͬ���٢ڢ���������Һ�������������һԪ�ᣬ�����Ƕ�Ԫ�ᣬ�ֱ�����ͬŨ�ȵ��ռ���Һǡ����ȫ��Ӧ�������ռ�������Ϊ1��1��2�������������ǿ�ᣬ���������ᣬ����ǿ����ˮ���Լ��ԣ�ǿ��ǿ���β�ˮ�⣬��Һ�����ԣ�������Һ��pH��С��ϵΪ������=�����ʴ�Ϊ��1��1��2��������=����
��5�����ݵ���غ㣺c(Cl-)=2c(Fe2+)+3c(Fe3+)+c(H+)(������Һ��OH-Ũ�Ⱥ�С����������Ժ��Բ���)����c(H+)=c(Cl-)-2c(Fe2+)-3c(Fe3+)=1.0��10-2molL-1������ҺpH=-lg1.0��10-2=2���ʴ�Ϊ��2��
��6��FeCl3ˮ�����ɵ���������������������ԣ��ܹ�����ˮ�е��������ˮ�����ã����ӷ���ʽΪFe3+ + 3H2O![]() FeOH)3 (����)+ 3H+��FeCl3��Һ�е�����Ũ�ȴӴ�С˳��Ϊc(Cl-)> c(Fe3+)>c(H+)> c(OH-)���ʴ�Ϊ��Fe3+ + 3H2O
FeOH)3 (����)+ 3H+��FeCl3��Һ�е�����Ũ�ȴӴ�С˳��Ϊc(Cl-)> c(Fe3+)>c(H+)> c(OH-)���ʴ�Ϊ��Fe3+ + 3H2O![]() FeOH)3 (����)+ 3H+��c(Cl-)> c(Fe3+)>c(H+)> c(OH-)��
FeOH)3 (����)+ 3H+��c(Cl-)> c(Fe3+)>c(H+)> c(OH-)��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧҩƷ�İ�ȫ��ʾ��ע����ȷ����
A����ҵ�ƾ������綾Ʒ B������������ȼƷ
C��Ũ���������ױ�Ʒ D������������ʴƷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D�ĸ�ͬѧ�ij�����ȫ��ȷ���ǣ� ��
A.NaCl���������ӻ�������м��Լ�
B.H2O����1mol�к���2mol�Ǽ��Լ�
C.KOH���Ⱥ������Ӽ����ֺ��м��Թ��ۼ�
D.NaNO3�����Ǻ������Ӽ��Ĺ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ������ʵ�У���������������ԭ����ʾ����
A������ơ��ƿ��ƿ�����Ϸ��������ĭ
B����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ����
C��ʵ�����г����ű���ʳ��ˮ�ķ����ռ�Cl2
D����ҵ����������Ĺ�����ʹ�ù����Ŀ��������SO2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ����
A. ����ϩ����������ܷ����ӳɷ�Ӧ
B. �����ͺ������Ͷ��ǿ������ı�������
C. ��Ȼ����ˮú������Ҫ�ɷֶ�������
D. ����ʽΪC10H14�ĵ�ȡ������������ܵĽṹ��4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֪Ԫ���У���̬ԭ�ӵ�4s�ܼ���ֻ��1��������λ��d����Ԫ�ع��У� ��
A. 0�� B. 3�� C. 2�� D. 1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ����Ʊ���ȩ��ͬʱ�ܻ�õ��ܣ����ܷ�ӦΪ��2CH2�TCH2+O2��2CH3CHO�������й�˵������ȷ����( )
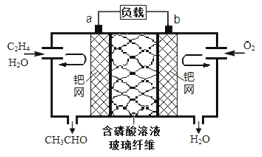
A���õ�ؿɽ���ѧ��ת��Ϊ����
B��ÿ��0.1mol O2��Ӧ����Ǩ��0.4mol H+
C��������ӦʽΪ��CH2=CH2-2e-+2OH-�TCH3CHO+H2O
D����������Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʶ����ʱ���Բ�ȡ���ַ���������й��� H2SO4 �ķ����ȷ����
A����Ԫǿ�� B������� C�������� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵���У���ȷ����
�������غͼ�ȩ����ȩ��֬�����ӳɷ�Ӧ�����۷�Ӧ��
����״���£�22.4 L��ȩ����������ԼΪ16 NA ��
���״�ͨ����һ���ж����壬������ֻ�����Լ�
��������̼������Һ�ķ�Ӧ��![]() [
[
��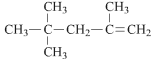 ������Ϊ��2,2,4-����-4-��ϩ
������Ϊ��2,2,4-����-4-��ϩ
��3-��-1-��ϩ�е�����̼ԭ�Ӳ����ܴ���ͬһƽ��
A���٢ڢܢ� B���ڢܢ� C���ڢ� D���٢ۢݢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com