
|
标准状况下,m1 g气体A与m2 g气体B的分子数相等,下列说法中正确的是 | |
| [ ] | |
A. |
1个A分子的质量是1个B分子的质量的 |
B. |
同温同体积的A与B的质量比为 |
C. |
同温同质量的A与B的分子数比为 |
D. |
同温同压下A与B的密度比为 |
科目:高中化学 来源: 题型:
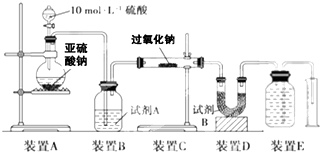
| 7m1 |
| 30 |
| 7m1 |
| 30 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

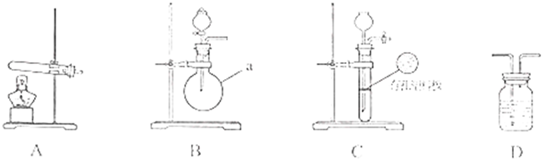
| 实验装置 | 实验药品 | 制备原理 | |||||||||
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① (NH4)2SO4+Ca(OH)2
(NH4)2SO4+Ca(OH)2
| ||||||||
| 乙小组 | ② B B |
浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③ 氢氧化钠溶于氨水后放热、增加氢氧根浓度,使NH3+H2O?NH3?H2O?NH4++OH-向逆方向移动,加快氨气逸出 氢氧化钠溶于氨水后放热、增加氢氧根浓度,使NH3+H2O?NH3?H2O?NH4++OH-向逆方向移动,加快氨气逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
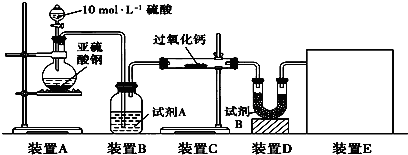
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com