
【题目】锗![]() 是典型的半导体元素,在电子、材料等领域应用广泛
是典型的半导体元素,在电子、材料等领域应用广泛![]() 回答下列问题:
回答下列问题:
(1)基态Ge原子的核外电子排布式为![]() ______,有______个未成对电子.
______,有______个未成对电子.
(2)![]() 与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键
与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键![]() 从原子结构角度分析,原因是______.
从原子结构角度分析,原因是______.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______.
|
|
| |
熔点 |
| 26 | 146 |
沸点 |
| 186 | 约400 |
(4)光催化还原![]() 制备
制备![]() 反应中,带状纳米
反应中,带状纳米![]() 是该反应的良好催化剂
是该反应的良好催化剂![]() 、Ge、O电负性由大至小的顺序是______
、Ge、O电负性由大至小的顺序是______
![]() 单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
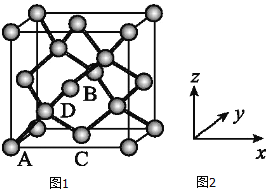
(6)晶胞有两个基本要素: ![]() 原子坐标参数,表示晶胞内部各原子的相对位置,如图
原子坐标参数,表示晶胞内部各原子的相对位置,如图![]() 、
、![]() 为Ge单晶的晶胞,其中原子坐标参数A为
为Ge单晶的晶胞,其中原子坐标参数A为![]() ;B为
;B为![]() ;C为
;C为![]() 则D原子的坐标参数为______.
则D原子的坐标参数为______.
![]() 晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数
晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数![]() ,其密度为______
,其密度为______ ![]() 列出计算式即可
列出计算式即可![]() .
.
【答案】 ![]() 2 锗的原子半径大,原子之间形成的
2 锗的原子半径大,原子之间形成的![]() 单键较长,
单键较长, ![]() 轨道肩并肩重叠程度很小或几乎不能重叠,难以形成
轨道肩并肩重叠程度很小或几乎不能重叠,难以形成![]() 键
键 ![]() 、
、![]() 、
、![]() 熔、沸点依次增高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强
熔、沸点依次增高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强 ![]()
![]() 共价键
共价键 ![]()
![]()
【解析】试题分析:(1)Ge原子核外有32个电子,根据能量最低原理分析核外电子排布;根据洪特规则分析未成对电子数;(2)锗的原子半径大, ![]() 轨道肩并肩重叠程度很小或几乎不能重叠,难以形成
轨道肩并肩重叠程度很小或几乎不能重叠,难以形成![]() 键; (3)
键; (3) ![]() 、
、![]() 、
、![]() 都是分子晶体,相对分子质量依次增大,分子间相互作用力逐渐增强;(4)非金属性越强,电负性越大;(5)金刚石是原子晶体,C原子杂化方式是
都是分子晶体,相对分子质量依次增大,分子间相互作用力逐渐增强;(4)非金属性越强,电负性越大;(5)金刚石是原子晶体,C原子杂化方式是![]() ;(6)
;(6)![]() 根据三维坐标分析C原子的坐标位置;
根据三维坐标分析C原子的坐标位置; ![]() 根据均摊原则计算晶胞中原子数,根据
根据均摊原则计算晶胞中原子数,根据![]() 计算晶胞密度;
计算晶胞密度;
解析:(1)Ge原子核外有32个电子,根据能量最低原理,核外电子排布式是![]() ;根据洪特规则,2P轨道的2个电子都是未成对电子;(2)锗的原子半径大,原子之间形成的
;根据洪特规则,2P轨道的2个电子都是未成对电子;(2)锗的原子半径大,原子之间形成的![]() 单键较长,
单键较长, ![]() 轨道肩并肩重叠程度很小或几乎不能重叠,难以形成
轨道肩并肩重叠程度很小或几乎不能重叠,难以形成![]() 键,所以C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键;(3)
键,所以C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键;(3) ![]() 、
、![]() 、
、![]() 熔、沸点依次增高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强;(4)非金属性越强电负性越大,非金属性
熔、沸点依次增高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强;(4)非金属性越强电负性越大,非金属性![]() ,所以电负性
,所以电负性![]() ;(5)
;(5)![]() 单晶具有金刚石型结构,金刚石中C原子杂化方式是
单晶具有金刚石型结构,金刚石中C原子杂化方式是![]() ,所以Ge原子的杂化方式为
,所以Ge原子的杂化方式为![]() ,锗原子之间存在的作用力是共价键;(6)
,锗原子之间存在的作用力是共价键;(6)![]() 根据三维坐标,C原子的坐标位置是
根据三维坐标,C原子的坐标位置是![]() ;
; ![]() 根据均摊原则,晶胞中锗原子数是
根据均摊原则,晶胞中锗原子数是![]() ,晶胞的摩尔质量是
,晶胞的摩尔质量是![]() ,根据
,根据![]() ,晶胞密度是
,晶胞密度是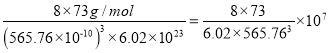
![]() ;
;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将一块金属钠投入到滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面
②钠立即与水反应,并有气体产生
③反应后溶液变红
④钠熔成闪亮的小球
⑤小球在水面上四处游动
⑥有“嘶嘶”的响声发出
A. ①②③④ B. ②③④⑤
C. ②④⑤⑥ D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。请回答下列问题。
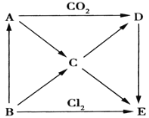
(1)固体A的名称为_______________,其常见用途:_______________________________________。(仅举一例即可)
(2)写出下列反应的化学方程式:
①A→C_____________________________________________________________;
②A→D_____________________________________________________________;
③B→A_____________________________________________________________;
④B→C_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某品牌饮用矿物质水标签的部分内容。下列说法正确的是

A. 标签上给出的离子的物理量是物质的量浓度
B. 任何饮用水中氯离子(Cl-)的浓度均在10~27.3 mg/L之间
C. 该品牌饮用矿物质水中c(Mg2+)的最大值为2×10-4 mol/L
D. 一瓶该品牌饮用矿物质水中SO42-的物质的量不超过1×10-5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置图或曲线图与对应的叙述相符的是
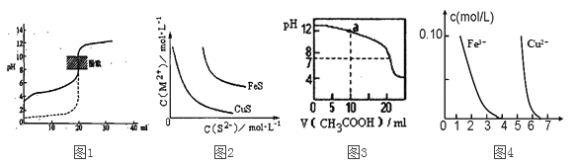
A. 如图1所示,用0.1mol/LNaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线
B. 某温度下FeS、CuS的沉淀溶解平衡曲线如图2所示,纵坐标c(M2+)代表Fe2+或Cu2+的浓度,横坐标c(S2—)代表S2—浓度。在物质的量浓度相等的Fe2+和Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为Fe2+
C. 如图3所示,用0.1mol/LCH3COOH溶液滴定20mL0.1mol/LNaOH溶液的滴定曲线,当pH=7时:c(Na+)=c(CH3COO—)>c(OH—)=c(H+)
D. 据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5.5左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中常用烧碱来清洗抽油烟机上的油渍(主要成分是油脂),下列说法不正确的是( )
A. 烧碱具有强腐蚀性,故清洗时必须戴防护手套
B. 热的烧碱溶液去油渍效果更好
C. 清洗时,油脂在碱性条件下发生水解反应
D. 油脂属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图实验装置制取干燥的气体正确的是

A | B | C | D |
大理石与盐酸 | 锌粒与稀硫酸 | 双氧水与二氧化锰 | 二氧化锰与氯酸钾 |
浓硫酸 | 浓硫酸 | 无水氯化钙 | 浓硫酸 |
CO2 | H2 | O2 | O2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要0.2 mol·L-1 NaCl溶液240 mL,配制流程如下:
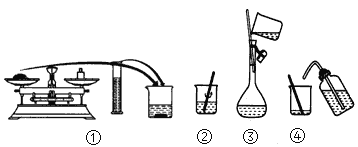

回答下列问题:
(1)①中称得________gNaCl。
(2)玻璃棒在②③两步中的作用分别是____________、______________。
(3)某同学在第⑧步观察液面时俯视,所配溶液浓度______(填“偏高”“偏低”或“无影响”)。
(4)容量瓶在使用之前要__________,具体操作是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以惰性电极电解下列物质的水溶液(电解质均过量),电解后溶液pH升高的是( )
①盐酸 ②硫酸 ③氢氧化钾 ④氯化钾 ⑤硝酸银 ⑥硫酸钠
A. ①②③ B. ④⑤⑥ C. ①③④ D. ②⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com