
【题目】银的冶炼有很多方法,在《天工开物》均有记载,而现代流行的“氰化法”,即 用NaCN溶液浸出矿石中的银的方法是常用的方法。该方法具备诸多优点:银的回收率高、对游离态和化合态的银均能浸出、对能源消耗相对较少,生产工艺简便等,但银化物通常有毒。其炼制工艺简介如下:
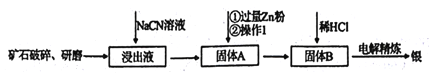
(1)矿石需要先进行破碎、研磨,其目的是_________。
(2)写出该工艺的一个明显的缺点____________。
(3)用NaCN浸泡矿石(该矿石是辉银矿,其主要成分是Ag2S)时,反应容器处于开口状态,产生的银以[Ag(CN)2]-形式存在,硫元素被氧化至最高价,试写出主要反应的离子方程式________。
(4)银往往和锌、铜、金等矿伴生,故氰化法得到的银中往往因含有上述金属而不纯净,需要进一步纯化,从而获得纯净的银。其中方法之一就是进行电解精炼,在精炼过程中,含有杂质的银作_______极(填“阴”或“阳”),该电极上发生的主要反应式为_____。
(5)有人提出了另外的提纯银的方案,先将锌粉还原后的混合金属用略过量的硝酸溶解,通 过精确调整溶液的pH来进行金属元素逐一分离,已知:
①溶解后的离子浓度如表:
Zn2+ | Cu2+ | Ag+ | |
物质的量浓度(mol/L) | 0.001 | 0.002 | 0.5 |
②某些金属离子的氢氧化物Ksp如表:
Zn2+ | Cu2+ | Ag+ | …… | |
Ksp | 1.0×10-17 | 2.0×10-20 | 2.0×10-8 |
(已知lg2=0.3),该设计方案 ______(填“可行”或“不可行”),其原因是______________。
【答案】增大接触面积,增大反应速率(提高浸出率) NaCN有毒(生成有毒HCN),生产环节不环保,对环境不友好等 Ag2S+4CN-+2O2=2[Ag(CN)2]-+SO42- 阳 Ag-e-=Ag+ 不可行 在调整pH的过程中,各离子的沉淀pH接近,难以逐一沉淀
【解析】
(1)从固态物质对化学反应速率及物质利用率分析;
(2)根据氰化物是有毒物质分析;
(3)根据题意,结合电子守恒、电荷守恒及原子守恒书写方程式;
(4)在金属精炼过程中,不纯金属作阳极,发生氧化反应;
(5)根据溶液中各种离子浓度大小及金属氢氧化物的溶度积常数计算形成沉淀需要的c(OH-)大小分析判断。
(1)矿石是块状固态,将其粉碎、研磨,就可以增大与其他反应物的接触面积,从而可以提高化学反应速率,使更多的物质反应,提高了原料的浸出率;
(2)该冶炼金属银的方法使用了剧毒物质NaCN,对周围环境和操作人员都会形成危害,最后的排出物也容易形成对环境的污染,所以对环境不友好;
(3)用NaCN浸泡矿石(其主要成分是Ag2S)时,反应容器处于开口状态,空气中O2会进入到反应溶液中,产生的银以[Ag(CN)2]-形式存在,硫元素被氧气氧化至最高价的SO42-,根据电子守恒、电荷守恒及原子守恒,可得主要反应的离子方程式为:Ag2S+4CN-+2O2=2[Ag(CN)2]-+SO42-;
(4) 氰化法得到的银中含有杂质,需电解精炼,在精炼过程中,含有杂质的银与电源的正极连接作阳极,阳极发生氧化反应,主要反应式为Ag-e-=Ag+,活动性比Ag强的金属也会失去电子,如Zn-2e-=Zn2+、Cu-2e-=Cu2+;
(5)根据Ksp[Zn(OH)2]=c(Zn2+)c2(OH-)=1.0×10-17,0.001×c2(OH-)=1.0×10-17,c(OH-)=1.0×10-7;
根据Ksp[Cu(OH)2]=c(Cu2+)c2(OH-)=2.0×10-20,0.002×c2(OH-)=2.0×10-20,c(OH-)=3.2×10-9;
根据Ksp(AgOH)=c(Ag+)c(OH-)=2.0×10-8,0.5×c(OH-)=2.0×10-8,c(OH-)=4.0×10-8.可见各种离子形成沉淀需要的pH非常接近,难以逐一沉淀,因此该方法不可行。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】I、 向KI和硫酸混合溶液中加入过氧化氢溶液,迅速反应放出大量气泡,溶液呈棕色。
查阅资料知,反应过程如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)用双线桥法表示过程①电子转移情况:H2O2+2KI+H2SO4=I2+K2SO4+2H2O_____________。
(2)只比较上述反应②与③,则判断I2起到了___________的作用。
(3)试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:___________(填化学式)。
II、一定条件下,向含硝酸的废水中加入CH3OH(碳元素为-2价),将HNO3还原成N2。若参加反应的还原剂和氧化剂的物质的量之比是5∶6,则该反应中被氧化的元素的化合价为_____;每转移3 mol电子,反应消耗_____g CH3OH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2O(g)=2 H2(g)+O2(g) ΔH=+496kJ·mol-1 。断开1 mol H—H键、O=O键分别需要吸收436 kJ、498 kJ的热量,则断开1 molO—H键需要吸收的热量为( )
A. 462 kJB. 469 kJC. 362 kJD. 466.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗,其制备过程如图所示,下列叙述不合理的是
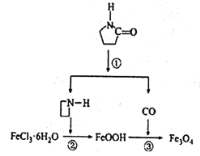
A. 在反应②中,![]() 的作用可能是促进氯化铁水解
的作用可能是促进氯化铁水解
B. 直接加热FeCl3溶液也可以得到Fe3O4
C. 反应③的化学方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
D. 纳米四氧化三铁形成的分散系,有可能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车的启动电源常用铅蓄电池,电池反应如下: PbO2 + Pb + 2H2SO4 ![]() 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
A. PbO2放电时是电池的负极,充电时是电池的阳极
B. 负极的电极反应式为:Pb + SO42—– 2e–=PbSO4
C. 放电时,PbO2得电子,被氧化
D. 电池放电时,溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为从海带中提碘生产的实验室模拟流程。试回答下列问题:
(1)实验操作中所用玻璃仪器为酒精灯、烧杯、普通漏斗、牛角管、锥形瓶、蒸馏烧瓶等。若要完成操作1,还缺少的玻璃仪器有 ,该仪器的作用为 ;操作2的名称为 ;若要完成操作3,还缺少的玻璃仪器有 。
(2)实验室用二氧化锰制氯气的化学方程式为 。
(3)弃液B中滴入淀粉液,溶液呈蓝色,但通入二氧化硫后蓝色褪去,写出该过程中发生反应的化学方程式并用双线桥标明电子转移的方向和数目 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A.950 mL,111.2 gB.500 mL,117 g
C.1 000 mL,117 gD.任意规格,111.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:
A 金刚石与石墨;B 淀粉与纤维素;C 氕与氘;D 甲烷与戊烷; E 葡萄糖与果糖
F![]() 与
与 G
G  与
与
其中互为同位素 _____;(填编号.下同),互为同系物的是____,互为同分异构体的是______,是同一种物质的是________.
(2)化合物A的结构简式为: ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_____;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为_____。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_____;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为_____。
(3)篮烷分子的键线式如图所示,试回答:

写出篮烷分子的化学式________;篮烷分子的一氯取代物的种数为______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素,它们在元素周期表中的相对位置如图所示,其中B的单质在空气中含量约占80%。
A | B | C | |||
D |
(1)写出下列元素的名称:C____,D___。
(2)画出B的原子结构示意图____。C在元素周期表中的位置是____。
(3)B、C两种元素最简单氢化物的稳定性由强到弱的顺序是_____。写出A的最简单氢化物的电子式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com