
已知反应:2SO2(g)+O2(g)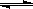 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
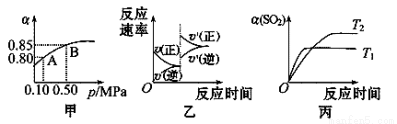
A.由图甲知,B点SO2的平衡浓度为0.3mol·L-1
B.由图甲知,A点对应温度下的平衡常数为80
C.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
D.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源:2014-2015上海市奉贤区高三第二学期调研测试化学试卷(解析版) 题型:选择题
Na2O2、Cl2和SO2均能使品红溶液褪色(NA为阿伏加德罗常数的值)。下列说法正确的是
A.Na2O2、Cl2、SO2使品红溶液褪色的原理相同
B.标准状况下,1 mol Na2O2和22.4LCO2反应,转移电子数目为NA
C.等物质的量的Cl2和SO2同时通入品红溶液中,品红褪色更快
D.在Na2O2中阴阳离子所含的电子数目相等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省张掖市高三4月诊断考试理综化学试卷(解析版) 题型:实验题
(13分)重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下:
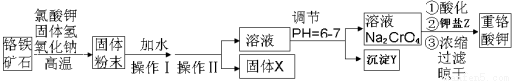
试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有 。铁在周期表的位置是 。
(2)操作Ⅱ的名称是 。
(3)固体X的主要成分是___________,沉淀Y的主要成分是 。
(4)流程中①酸化所用的酸和②钾盐Z最合适的是(填符号)________,
A.盐酸和氯化钾 B.硫酸和氯化钾
C.硫酸和硫酸钾 D.次氯酸和次氯酸钾
酸化反应的离子方程式为 。
(5)FeO·Cr2O3与氯酸钾、氢氧化钠高温反应化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
己烯雌酚是一种激素类药物,结构如下。下列有关叙述中不正确的是
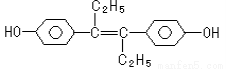
A.它易溶于有机溶剂
B.可与NaOH和NaHCO3发生反应
C.1mol该有机物可以与5mol Br2发生反应
D.该有机物分子中,一定有12个碳原子共平面
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是
2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
2 min末浓度/mol·L-1 | 0.08 | a | b |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.前2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 mol·L-1·min-1
D.增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:填空题
(16分)请根据官能团的不同对下列有机物进行分类。
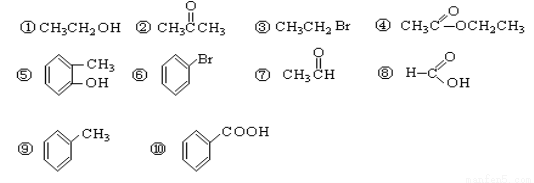
(1)芳香烃: ; (2)卤代烃: ;
(3)醇: ; (4)酚: ;
(5)醛: ; (6)酮: ;
(7)羧酸: ; (8)酯: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:选择题
根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:简答题
(12分)二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
①CO(g) + 2H2(g)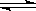 CH3OH(g) △H1=-Q1 kJ·mol-1
CH3OH(g) △H1=-Q1 kJ·mol-1
②2CH3OH(g)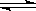 CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
③CO(g)+ H2O(g)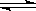 CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
回答下列问题:
(1)新工艺的总反应3H2(g)+ 3CO(g)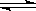 CH3OCH3(g)+ CO2(g)的热化学方程式为 。
CH3OCH3(g)+ CO2(g)的热化学方程式为 。
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g) + 2H2(g) 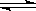 CH3OH (g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(Κ)。
CH3OH (g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(Κ)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断ΔH 0 (填“ >”、“=”或“<”)。能够说明某温度下该反应是平衡状态的是 。
A.体系的压强不变 B.密度不变
C.混合气体的相对分子质量不变 D.c(CO)=c(CH3OH)
②某温度下,将 2mol CO和 6mol H2 充入2L的密闭容器中,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K= 。
(3)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨。合成氨反应原理为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJmol-1。实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1。请回答下列问题:
2NH3(g) ΔH=-92.4kJmol-1。实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1。请回答下列问题:
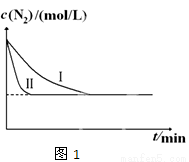
①与实验Ⅰ比较,实验Ⅱ改变的条件为 。
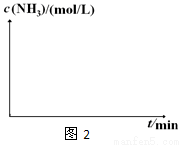
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在图2中画出实验Ⅰ和实验Ⅲ中c(NH3)随时间变化的示意图。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高一下学期第一次月考化学试卷(解析版) 题型:选择题
离子RO42-中,有x个核外电子,R质量数为A,则R原子核内含有的中子数目为
A.A-x+48 B.A-x+24 C.A-x+34 D.A-x-24
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com