
【题目】1个某种氯原子的质量是a g,1个12C原子的质量是b g,用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
①该氯原子的相对原子质量为12a/b ②m g该氯原子的物质的量为m/(aNA) mol ③该氯原子的摩尔质量是aNA g ④a g该氯原子所含的电子数为17 mol
A.①②B.①③C.②③D.②④
【答案】A
【解析】
①某原子的相对原子质量等于一个该原子的质量除以一个12C原子质量的十二分之一,据此计算氯原子的相对原子质量;
②一个氯原子的质量为ag,则NA个氯原子的质量为aNAg,则氯原子的摩尔质量为aNAg/mol,再依据n=m/M计算物质的量;
③摩尔质量的单位为g/mol;
④某氯原子的质量是ag,则ag该氯原子即1个,据此分析。
①氯原子的相对原子质量为一个氯原子的质量除以一个12C原子质量的十二分之一,即氯原子的相对原子质量=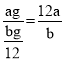 ,①正确;
,①正确;
②一个氯原子的质量为ag,NA个氯原子的质量为aNAg,则氯原子的摩尔质量为aNAg/mol,所以mg该氯原子的物质的量为![]() ,②正确;
,②正确;
③一个氯原子的质量为ag,NA个氯原子的质量为aNAg,则氯原子的摩尔质量为aNAg/mol,③错误;
④某氯原子的质量是ag,则ag该氯原子即1个氯原子,含17个电子,④错误;
综上所述,①②正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大。
(1)试推断A、B、C、D四种元素的符号:A________、B________、C________、D________。
(2)写出A元素原子的核外电子排布式:____________;写出B元素原子核外电子排布的价电子构型:__________;用电子排布图表示C原子的核外电子排布情况:_______________。
(3)比较四种元素的第一电离能和电负性的大小:第一电离能____________;电负性____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素下列说法不正确的是( )
![]()
A. Y的最高价氧化物对应水化物的酸性比X的弱
B. Z位于元素周期表中第二周期,第ⅥA族
C. X的气态氢化物的稳定性比Z的弱
D. M的原子半径比Y的原子半径大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学–选修3:物质结构与性质)碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(1)在第二周期的元素中,第一电离能介于B与N之间的元素有_________种。
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是_____________。
(3)Fe与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为______________。请写出一个与CO互为等电子体的离子:________________。

(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Gr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH氧化成CH3COOH,试写出基态铬原子的价层电子排布式__________;CH3COOH分子中碳原子的杂化类型为___________。
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为_______,NH3的VSEPR模型为_______。
③铜铬合金的晶胞如图所示,已知晶胞中Cr和Cu原子间的最近距离为![]() apm,则该晶体的密度为_______g·cm-3(用含a的代数式表示,设NA为阿伏加德罗常数的值)。
apm,则该晶体的密度为_______g·cm-3(用含a的代数式表示,设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究实验室制乙烯及乙烯和溴水的加成反应。甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的。乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:

(1)写出甲同学实验中两个主要反应的化学方程式:________________________;________________________
(2)乙同学认为因刺激性气体的存在不能认为溴水褪色是乙烯的加成反应造成的。原因是(用化学方程式表示):____________________________________
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净):发现最后气体经点燃是蓝色火焰,确认有一氧化碳。

①设计装置a的作用是________________________________________________
②浓氢氧化钠的作用是____________________________________
③浓溴水的作用是________________________
④稀溴水的作用是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧铅蓄电池的回收利用可减少对环境的污染和实现铅资源的可持续发展,其阴、阳极填充物(铅膏,主要含PbO2、PbO、PbSO4)是废旧铅蓄电池的主要部分,回收铅单质的一种工艺流程如下:

(1)反应①的化学方程式为________________,操作a的名称是___________。
(2)滤液B中的溶质除Na2SO4外,还含有较多的___________(写化学式),若利用该滤液回收Na2SO4·10H2O,可加入___________(写试剂名称)除掉该物质。
(3)若反应②完成后的溶液中c(Pb2+)=5×10-6mol/L,则该溶液中c(SO42-)<___________ mol/L [已知Ksp(PbSO4)=1.06×10-8,Ksp (PbCO3)=3.3×10-14]
(4)用涂PbO2的钛板作阳极,铅板作阴极,电解含Pb2+的电解液,可得到纯度99.99%的Pb粉,产物Pb在___________极(填“阴”或“阳”)产生,阳极的电极反应式为___________。
(5)若实验中所取铅膏的质量为16g(PbO2的质量分数为15%),要将PbO2全部还原,至少需要加入1.0mol/L的Na2SO3溶液___________ mL(结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置如下图所示,Y2+与W-的电子数之差为8。下列说法正确的是

A. 原子半径大小:X>Y
B. 最高价氧化物对应水化物的酸性:Z>W
C. 工业上通过电解Y的氧化物制取Y单质
D. X与W可形成正四面体结构的有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在一定条件下发生反应:A+B=C+D,14gA和9gB恰好完全反应生成0.5molC和1gD则物质C的摩尔质量为____________;
(2)某1L混合溶液中所含离子的个数比如下表,则M离子可能为(_______)
所含离子 | NO3- | SO42- | Cu2+ | M |
个数比 | 4 | 1 | 2 | 1 |
A.Ba2+ B.Mg2+ C.Cl- D.Na+
(3)已知a g气体X2中含有b个X原子,那么c g该气体在标准状况下的体积是____________;
(4)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使SO![]() 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为________。
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. 体系压强不再变化 D. 2v逆(X)=v正(Y)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com