
| Ԫ�ر�� | Ԫ �� �� �� �� Ϣ |
| A | �����������Ǵ�����������2�� |
| B | ��Eͬ���� |
| C | 1mol C����������ˮ��Ӧ���ڱ�״��������11.2L H2 |
| D | ԭ�������������������������� |
| E | ��һ�������ӵĵ��Ӳ�ṹ��Arԭ����ͬ |
 ��E�����ڱ��е�λ��Ϊ���������ڵڢ�A�壮
��E�����ڱ��е�λ��Ϊ���������ڵڢ�A�壮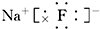 ��
������ ������Ԫ��A��B��C��D��E��ԭ�������������������������Ǵ�����������2������AΪCԪ�أ�1mol C����������ˮ��Ӧ���ڱ�״��������11.2L H2����CΪNaԪ�أ�D��ԭ��������������������������������D��ԭ����������Na����DΪ�������ڵڢ�A��Ԫ�أ�����DΪAlԪ�أ���һ�������ӵĵ��Ӳ�ṹ��Arԭ����ͬ����EΪClԪ�أ�B��Eͬ���壬����BΪFԪ�أ���ϻ�ѧ���PԪ�������������
��� �⣺������Ԫ��A��B��C��D��E��ԭ�������������������������Ǵ�����������2������AΪCԪ�أ�1mol C����������ˮ��Ӧ���ڱ�״��������11.2L H2����CΪNaԪ�أ�D��ԭ��������������������������������D��ԭ����������Na����DΪ�������ڵڢ�A��Ԫ�أ�����DΪAlԪ�أ���һ�������ӵĵ��Ӳ�ṹ��Arԭ����ͬ����EΪClԪ�أ�B��Eͬ���壬����BΪFԪ�أ�
��1��DΪAlԪ�أ���ԭ�Ӻ�����13�����ӣ�ԭ�ӽṹʾ��ͼΪ�� ��EΪClԪ�أ������ڱ���λ�ڵ������ڣ���VIIA�壻
��EΪClԪ�أ������ڱ���λ�ڵ������ڣ���VIIA�壻
�ʴ�Ϊ�� ���������ڵڢ�A�壻
���������ڵڢ�A�壻
��2��Na��F�γ����ӻ�����NaF�������ʽΪ��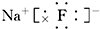 ���ʴ�Ϊ��
���ʴ�Ϊ��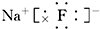 ��
��
��3�������Ų���ͬ�����ӣ�ԭ������Խ�����Ӱ뾶ԽС�����뾶��F-��Al3+��
�ʴ�Ϊ��F-��Al3+��
��4�����������������ʣ�����ɫ��״̬�����ȽϷǽ����ԣ��������⻯����ȶ��ԡ����������ϵ����׳̶ȡ������ӵĻ�ԭ�ԡ�����������Ӧˮ��������Ի�Ԫ�������ڱ���λ�õ����ȽϷǽ����ԣ�
�ʴ�Ϊ��ae��
��5��ClԪ��������������Ԫ���е�һ��Ԫ���γɹ��ۻ���������е�ԭ�Ӹ�����1��4����Է�������Ϊ154��������ʵĻ�ѧʽΪCCl4���ʴ�Ϊ��CCl4��
���� ���⿼��λ�á��ṹ�����ʵĹ�ϵ��Ӧ�ã���ȷԪ�ص������ƶϳ���Ԫ���ǽ����Ĺؼ�������ϤԪ�ؼ��仯�������������ɣ���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������


 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ������Һ��Mg2+��K+��SO42-��NO3- | |
| B�� | ʹ��̪���ɫ����Һ��Na+��Cu2+��HCO3-��NO3- | |
| C�� | 0.1mol•L-1AgNO3��Һ��H+��K+��SO42-��I- | |
| D�� | 0.1mol•L-lNaAlO2��Һ��H+��Na+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��Һ��ͨ�����SO2��SO2+2OH-�TSO32-+H2O | |
| B�� | п��ϡ���ᷴӦ��Zn+2H+�TZn2++H2�� | |
| C�� | ���Ȼ�淋���Һ�м�������ŨKOH��Һ�����ȣ�NH4++OH- $\frac{\underline{\;\;��\;\;}}{\;}$NH3•H2O | |
| D�� | ����ˮ��ͨ��SO2���壺Cl2+SO2+2H2O�T4H++2Cl-+SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | PCl3 | C�� | PCl5 | D�� | H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��������B��A��D��C | B�� | ԭ�Ӱ뾶��A��B��C��D | ||
| C�� | �����ԣ�A��B���ǽ����ԣ�C��D | D�� | ���Ӱ뾶��D2-��C-��B2+��A+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
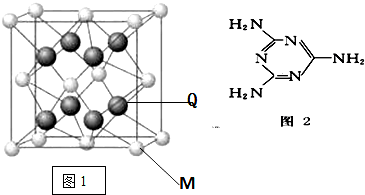
 ��ϩ�ǽ���ϳɵ�һ���л�����ķ��ӽṹ������ͼ��ʾ������̼����ԭ�Ӿ�����ȥ�������������ϩ��˵��������ǣ�������
��ϩ�ǽ���ϳɵ�һ���л�����ķ��ӽṹ������ͼ��ʾ������̼����ԭ�Ӿ�����ȥ�������������ϩ��˵��������ǣ�������| A�� | ��ϩ�ķ��������е�̼ԭ�ӹ�һƽ�� | |
| B�� | ��ϩ�DZ���һ��ͬ���칹�� | |
| C�� | ��ϩ����ϩ�Ĺ�������ͬ | |
| D�� | ��ϩ������һ�������·����ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��H2��=0.3 mol•L-1•min-1 | B�� | v��N2��=0.05 mol•L-1•s-1 | ||
| C�� | v��N2��=0.2 mol•L-1•min-1 | D�� | v��NH3��=0.3 mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/min | 2 | 4 | 7 | 9 |
| n��H2O��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com