
����Ŀ��(1)������0.2 g H2�к���____��Hԭ�ӣ�2 mol CO(NH2)2�к�___mol C��___mol N��___mol H����״���£�44.8 L O2�����Ϊ___mol��
(2) 2.3 g Na�к�___mol e������������ˮ��Ӧ�в�����״���µ�H2___L��
(3) 0.4 mol Al2(SO4)3����Һ�У���__mol SO42����Al3�����ʵ���__0.8 mol(����>������<����������)��
���𰸡�0.2NA 2 4 8 2 1.1 1.12 1.2 <
��������
(1)�ȼ���0.2gH2�����ʵ��������жϺ���Hԭ�ӵ����ʵ�����1��CO(NH2)2�����к�1��Cԭ�ӡ�1��Oԭ�ӡ�2��Nԭ�ӡ�4��Hԭ�ӣ���ϸ���֮�ȵ������ʵ���֮�Ƚ�𣻸���n=![]() ���㣻
���㣻
(2)����n=![]() �����жϣ���������ˮ��Ӧ�Ļ�ѧ����ʽ�������������ʵ���������������
�����жϣ���������ˮ��Ӧ�Ļ�ѧ����ʽ�������������ʵ���������������
(3)����Al2(SO4)3�Ļ�ѧʽ������������ʵ�������Һ�е������ӻᷢ��ˮ�ⷴӦ���ݴ˷����жϡ�
(1)0.2gH2�����ʵ���Ϊ![]() =0.1mol������Hԭ�ӵ����ʵ���Ϊ0.2mol��������0.2NA��Hԭ�ӣ�1��CO(NH2)2�����к�1��Cԭ�ӡ�1��Oԭ�ӡ�2��Nԭ�ӡ�4��Hԭ�ӣ���2mol CO(NH2)2�к�2mol C��2mol��2=4mol N��2mol��4=8mol H����״���£�44.8 L O2�����Ϊ
=0.1mol������Hԭ�ӵ����ʵ���Ϊ0.2mol��������0.2NA��Hԭ�ӣ�1��CO(NH2)2�����к�1��Cԭ�ӡ�1��Oԭ�ӡ�2��Nԭ�ӡ�4��Hԭ�ӣ���2mol CO(NH2)2�к�2mol C��2mol��2=4mol N��2mol��4=8mol H����״���£�44.8 L O2�����Ϊ![]() =2mol���ʴ�Ϊ��0.2NA��2��4��8��2��
=2mol���ʴ�Ϊ��0.2NA��2��4��8��2��
(2)2.3gNa���ʵ���Ϊ![]() =0.1mol�����е�����Ϊ��0.1mol��11=1.1mol������2Na + 2H2O=2NaOH + H2������֪0.1mol����ˮ��Ӧ�������������ʵ���Ϊ��0.1mol��
=0.1mol�����е�����Ϊ��0.1mol��11=1.1mol������2Na + 2H2O=2NaOH + H2������֪0.1mol����ˮ��Ӧ�������������ʵ���Ϊ��0.1mol��![]() =0.05mol������µ����Ϊ��0.05mol��22.4L/mol=1.12L���ʴ�Ϊ��1.1��1.12��
=0.05mol������µ����Ϊ��0.05mol��22.4L/mol=1.12L���ʴ�Ϊ��1.1��1.12��
(3)n(SO42-)=3n[Al2(SO4)3]=0.4mol��3=1.2mol����Һ���������ܹ�����ˮ�ⷴӦ����Al3+���ʵ�����0.4mol��2=0.8mol���ʴ�Ϊ��1.2������


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ����ijŨ�����Լ�ƿ�ϵ��й����ݣ����ݱ�ǩ�ϵ��й����ݻش��������⣺
����
����ʽ��HCl
��Է���������36.5
�ܶȣ�1.19g/cm3
����������36.5��
��1����Ũ��������ʵ���Ũ����___mol/L��
��2��ȡ�����������Ũ����ʱ������������������ȡ����Ķ��ٶ��仯����___��
A����Һ��HCl�����ʵ��� B����Һ��Ũ��
C����Һ��Cl-����Ŀ D����Һ���ܶ�
��3��ijѧ��������Ũ���������ˮ����100mL���ʵ���Ũ��Ϊ2.00mol/L��ϡ���ᡣ
�ٸ�ѧ����Ҫ��ȡ___mL(����һλС��)����Ũ����������ơ�
����Ҫʹ�õ�ʵ�������У��ձ�������������Ͳ��__��___��
�����ƹ����У�����ʵ������������Ƶ�ϡ��������ʵ���Ũ���к�Ӱ��?(�ں�������д��ƫ��������ƫС��������Ӱ����)
a.����Ͳ��ȡŨ����ʱ����___��
b.������ƿ�еμ�����ˮ����ʱ����__��
c.ת��ǰ������ƿ�к�����������ˮ__��
��4��ȡ�����Ƶ�2mol/L��ϡ����50mL������������̼��ƹ��壬������Ƶñ�״���µ�CO2�������___�������Է�Ӧ�����е�����仯����������Һ��CaCl2�����ʵ���Ũ�ȣ���д��������̣���___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������MnO2��ҵ�Ʊ����Ժ�Mn2+��ˮ�������й���������֪��Ksp[Mn(OH)2]��1.9��10��13 �� Ksp(MnCO3)��2.2��10��11���ش��������⣺
(1)�ö��Ե缫���MnSO4��Һ���Ʊ�MnO2����������ӦʽΪ___________��
(2)��MnSO4��Һ�м���(NH4)2CO3��Һ��ȡMnCO3ʱ�����Mn(OH)2�����ܵ�ԭ���ǣ�MnCO3(s)��2OH��(aq) ![]() Mn(OH)2(s)��CO32-(aq)���÷�Ӧ��ƽ�ⳣ��K��_________(����һλС��)��
Mn(OH)2(s)��CO32-(aq)���÷�Ӧ��ƽ�ⳣ��K��_________(����һλС��)��
(3)��ˮ�е�Mn2+��Ҳ����NH4HSO4������Һ��pH������ʱ����100 mL 0.1 mol/L��NH4HSO4��Һ�еμ�0.1 mol/L NaOH��Һ��������Һ��pH������NaOH��Һ����Ĺ�ϵ��������ͼ��ʾ (��Ӧǰ����Һ������仯���Բ���) ��

a��c(NH4+)��c(NH3 .H2O)��__________mol��L��1 ��ͼ��a��b��c��d�ĸ��㣬ˮ�ĵ���̶�������__________��b�㣬��Һ�и�����Ũ���ɴ�С������˳����____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС����ȡ�κ���±��Ũ��Һ(����K����Mg2����Br����SO42����Cl����)����ȡ�ϴ������Ȼ��ؾ��弰Һ��(Br2)������������������̣����ڸ���������˵����ȷ���ǣ� ��

A.�����١��۶�Ӧ�ķֱ�����ȡ����Һ
B.��������Ҫ����Ҫ�����������ձ��⣬����Ҫ������ƿ
C.X��Y��Z ���Էֱ���BaCl2��KOH��K2CO3
D.Ҫ�õ��������Ȼ��ؾ��壬��������ɫ��ҺB�м���ϡ���������ԣ�Ȼ�������ᾧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S�ķֽⷴӦ��һ�����淴Ӧ���������뷴Ӧ���̵Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ������ ��
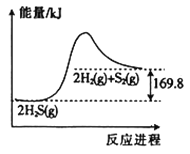
A. ����Ӧ�Ļ�ܴ����淴Ӧ�Ļ��
B. ����С��ϵ��ѹǿ����÷�Ӧ���ʱ佫����
C. �����¶�����ѧ��Ӧ���ʼӿ���H2S��ƽ��ת���ʼ�С
D. ���ܱ������г���1molH2S��ַ�Ӧ������84.9kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ����
A.H2SO4+2NaOH��Na2SO4+2H2O
B.CuO+H2![]() Cu+H2O
Cu+H2O
C.Cu2(OH)2CO3 ===2CuO+ CO2��+H2O
D.CuSO4+H2S===CuS��+H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д����ȷ����
A. ���ҽ���Һ�м������ᡢ˫��ˮ��2I����2H����H2O2===I2��2H2O
B. ̼��������Һ����������������Һ��ϣ�HCO3-��Ba2����OH��===BaCO3����H2O
C. ��Al2(SO4)3��Һ�м�������İ�ˮ��Al3����4NH3��H2O===AlO2-��4NH4+��2H2O
D. ��������������̼����������ⱥ���Ȼ�����Һ��2Cl����2H2O![]() H2����Cl2����2OH��
H2����Cl2����2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�о����֣����и߶ȶԳƵ��л����Ӿ��������Ըߣ��ȶ���ǿ�������ܴ���ص㣬�����Щ���ӳ�Ϊ��ѧ���ע���ȵ㡣������������һϵ�жԳƽṹ�������磺![]() (����������C4H4)��
(����������C4H4)��![]() (�⾧��C6H6)��
(�⾧��C6H6)��![]() ������C8H8)�ȣ������й�˵����ȷ����
������C8H8)�ȣ������й�˵����ȷ����
A. ����������Cԭ�Ӷ��γ�4��������������Ƕ���������
B. ����һϵ�����ʻ�Ϊͬϵ����ǵ�ͨʽΪC2nH2n(n��2)
C. �⾧������������̼ԭ�Ӿ�Ϊ����̼ԭ�ӣ�����ȴ����������ͬ
D. ������ϩ(![]() )���⾧������ͬ���칹��
)���⾧������ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�ClO2��KClO3��H2C2O4��H2SO4![]() ClO2����K2SO4��CO2����H2O(δ��ƽ)����˵����ȷ����
ClO2����K2SO4��CO2����H2O(δ��ƽ)����˵����ȷ����
A.KClO3�ڷ�Ӧ�еõ�����B.ClO2����������
C.H2C2O4�ڷ�Ӧ�б���ԭD.1 mol KClO3�μӷ�Ӧ��2 mol����ת��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com