
(1)在100 g浓度为c mol·L-1、密度为ρ g·cm-3的硫酸中加入一定量的水稀释成 mol·L-1的硫酸,则加入水的体积________ 100 mL(填“=”、“>”或“<”,下同)。
mol·L-1的硫酸,则加入水的体积________ 100 mL(填“=”、“>”或“<”,下同)。
(2)若把(1)中的H2SO4改成氨水,应加入水的体积________________________________________________________________________
100 mL。
(3)若把(1)(2)中的物质的量的浓度均改为溶质的质量分数,则加入水的体积________ 100 mL。
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
A.常温下,1 L 0.1 mol·L-1 NH4NO3溶液中的氮原子数为0.2NA
B.含有58.5 g氯化钠的溶液中含有NA个氯化钠分子
C.在反应KIO3+6HI===KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
D.常温常压下,22.4 L乙烯中C—H的个数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
(1)混合气体的密度是________________________________________________________________________。
(2)混合气体的平均摩尔质量是________________________________________________________________________。
(3)CO2和CO的体积之比是________________________________________________________________________。
(4)CO的体积分数是________________________________________________________________________。
(5)CO2和CO的质量之比是________________________________________________________________________。
(6)CO的质量分数是________________________________________________________________________。
(7)混合气体中所含氧原子的物质的量是________________________________________________________________________。
(8)混合气体中所含碳原子的物质的量是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1(b-2a) mol·L-1
B.10(2a-b) mol·L-1
C.10(b-a) mol·L-1
D.10(b-2a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用“偏大”、“偏小”或“无影响”填空
(1)配制450 mL 0.1 mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8 g________。
(2)配制500 mL 0.1 mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0 g________。
(3)配制NaOH溶液时,天平的两个托盘上放两张质量相等的纸片,其他操作均正确________。
(4)配制一定物质的量浓度的NaOH溶液,需称量溶质4.4 g,称量时物码放置颠倒________。
(5)用量筒量取浓硫酸时,仰视读数________。
(6)配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容________。
(7)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线________。
(8)定容摇匀后,发现液面下降,继续加水至刻度线________________________________________________________________________。
(9)定容时仰视刻度线________。
(10)定容摇匀后少量溶液外流________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100 mL pH为2、浓度约为0.1 mol·L-1的NH4Al(SO4)2溶液,配制过程为
①用托盘天平称量NH4Al(SO4)2·12H2O固体________________________________________________________________________g;
②将上述固体置于烧杯中,________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒的核外电子的表示方法中正确的是( )
A.C 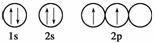
B.P原子价电子轨道表示式
C.Cr原子的价电子排布式 3d44s2
D.Fe2+ 1s22s22p63s23p63d64s2
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层电子数都达到8个电子的稳定结构。下列说法不正确的是( )

A.该化合物的化学式是Al2Cl6 B.该化合物是离子化合物,在熔融状态下能导电
C.该化合物在固态时所形成的晶体是分子晶体 D.该化合物中不存在离子键,也不含有非极性共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com