
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.请用元素符号或化学式填空:
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.请用元素符号或化学式填空: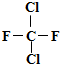 ,下列叙述正确的是:
,下列叙述正确的是:

科目:高中化学 来源: 题型:
 2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2
2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2| 高温 |
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 把1mol CH4 和一定量Cl2组成的混合气体通入大试管中,将此试管倒立在盛有饱和食盐水的水槽中,放在光亮处,回答下列问题:
把1mol CH4 和一定量Cl2组成的混合气体通入大试管中,将此试管倒立在盛有饱和食盐水的水槽中,放在光亮处,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
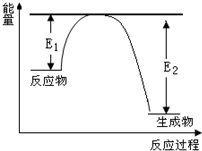
 (1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是
(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该材料中只存在极性共价键 |
| B、其储氢与放氢过程中只发生物质的变化 |
| C、组成硼氮--甲基环戊烷的四种元素中氮的第一电离能最大 |
| D、甲基环戊烷核磁共振氢谱有3种峰,且峰面积比为3:4:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱溶液去油污 |
| B、明矾可用于净水 |
| C、加热稀醋酸溶液其pH值减小 |
| D、小苏打溶液与AlCl3溶液混合产生气体和沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com