

分析 工业上生产Na3AlF6的主要流程:氟化钙、石英、纯碱高温煅烧:CaF2+Na2CO3 +SiO2$\frac{\underline{\;高温\;}}{\;}$ CO2↑+2NaF+CaSiO3↓,加水浸取,残渣为CaSiO3,加入硫酸铝,
硫酸铝与NaF(aq)反应的离子方程式为:3Na++6F-+Al3+=Na3AlF6↓,过滤、洗涤、干燥得纯净的Na3AlF6产品.
(1)根据CaF2+Na2CO3 +SiO2$\frac{\underline{\;高温\;}}{\;}$ CO2↑+2NaF+CaSiO3↓,可知浸取后的“残渣”中一定含有的成分是CaSiO3,硫酸铝与NaF(aq)反应生成Na3AlF6;
(2)煅烧后的固体在浸取前进行粉碎能提高NaF的浸出率,硫酸铝与NaF(aq)反应生成Na3AlF6沉淀,需先过滤后洗涤干燥得到纯净的Na3AlF6产品;
(3)硫酸铝为强酸弱碱盐,氟化钠为强碱弱酸盐,两者能发生双水解反应生成氢氧化铝沉淀;
(4)根据氟元素守恒进行解答,3CaF2~Na3AlF6;
(5)在偏铝酸钠及氟化钠溶液中,通入足量二氧化碳生成六氟铝酸钠沉淀和碳酸氢钠.
解答 解:(1)氟化钙、石英、纯碱高温煅烧:CaF2+Na2CO3 +SiO2$\frac{\underline{\;高温\;}}{\;}$ CO2↑+2NaF+CaSiO3↓,加水浸取,氟化钠溶于水,硅酸钙难溶于水,所以残渣一定为硅酸钙,硫酸铝与NaF(aq)反应生成Na3AlF6沉淀,离子反应为:3Na++6F-+Al3+=Na3AlF6↓,
故答案为:CaSiO3;3Na++6F-+Al3+=Na3AlF6↓;
(2)将块状固体进行粉碎能增大接触面积,煅烧后的固体在浸取前进行粉碎,浸取时能提高NaF的浸出率,硫酸铝与NaF(aq)反应生成Na3AlF6沉淀,分离固体、液体用过滤进行分离,沉淀表面有杂质需进行洗涤,然后进行干燥得到纯净的Na3AlF6产品,
故答案为:粉碎;过滤、洗涤、干燥;
(3)硫酸铝为强酸弱碱盐,氟化钠为强碱弱酸盐,两者能发生双水解反应,离子反应为:3F-+Al3++3H2O=3HF↑+Al(OH)3↓,为防止双水解发生,所以加入硫酸铝溶液前,需先用硫酸将NaF(aq)的pH下调至5左右,
故答案为:F-、Al3+发生双水解而生成氢氧化铝沉淀;
(4)78kg含CaF280%的氟石n(CaF2)=$\frac{78kg×80%}{78g/mol}$=8×102mol,生产过程中的每一步含氟物质均完全转化,根据氟元素守恒:3CaF2~Na3AlF6,n(Na3AlF6)=8×102mol×$\frac{1}{3}$,m(Na3AlF6)=nM=8×102mol×$\frac{1}{3}$×210g/mol=56kg,
故答案为:56kg;
(5)根据题干信息:碳酸化法也是工业制取Na3AlF6的一种方法,在偏铝酸钠及氟化钠溶液中,通入足量二氧化碳必生成六氟铝酸钠沉淀,根据原子守恒,反应为:6NaF+4CO2+NaAlO2+2H2O=Na3AlF6↓+4NaHCO3,
故答案为:6NaF+4CO2+NaAlO2+2H2O=Na3AlF6↓+4NaHCO3.
点评 本题考查了Na3AlF6的制备,涉及物质的分离与提纯、离子反应方程式的书写、化学计算,理解原理以及熟练综合应用元素化合物知识是解答关键,题目难度中等.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 ? NaOH H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 33.0 | - | 315 |
| 升华温度/℃ | - | - | 180 | 300 |
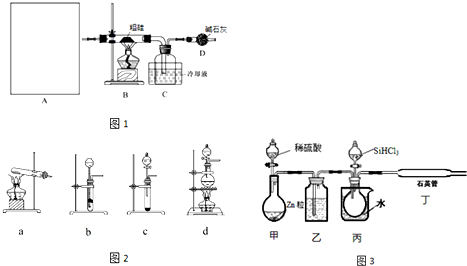
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 | |
| D. | 一定量氯气通入30 mL 10.00 mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com