
【题目】A、B、D、E、F、G是原子序数依次增大的六种短周期元素。A和B能形成B2A和B2A2两种化合物,B、D、G的最高价氧化物对应水化物两两之间都能反应,D、F、G原子最外层电子数之和等于15。回答下列问题:
(1)E元素在元素周期表中的位置是___________;A离子的结构示意图为____________。
(2)D的单质与B的最高价氧化物对应水化物的溶液反应,其离子方程式为________。
(3)①B2A2中含有___________键和___________键。
②该物质与水反应的化学反应方程式为___________________。
(4)下列说法正确的是____________(填字母序号)。
①B、D、E原子半径依次减小
②六种元素的最高正化合价均等于其原子的最外层电子数
③D的最高价氧化物对应水化物可以溶于氨水
④元素气态氢化物的稳定性:F>A>G
(5)在E、F、G的最高价氧化物对应水化物中,酸性最强的为__________(填化学式),用原子结构解释原因:同周期元素电子层数相同,从左至右,__________,得电子能力逐渐增强,元素非金属性逐渐增强。
【答案】 第三周期第IVA族 ![]() 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑ 离子 非极性共价 2Na2O2 + 2H2O = O2↑ + 4NaOH ① HClO4 半径逐渐减小
2Al + 2OH- +2H2O = 2AlO2- + 3H2↑ 离子 非极性共价 2Na2O2 + 2H2O = O2↑ + 4NaOH ① HClO4 半径逐渐减小
【解析】A、B、D、E、F、G是原子序数依次增大的六种短周期元素,A和B能形成B2A和B2A2两种化合物,A为O元素,B为Na元素;B、D、G的最高价氧化物对应水化物两两之间都能反应,D为Al元素;结合“D、F、G原子最外层电子数之和等于15”,则F为P元素,G为Cl元素,E为Si元素。
A、B、D、E、F、G是原子序数依次增大的六种短周期元素,A和B能形成B2A和B2A2两种化合物,A为O元素,B为Na元素;B、D、G的最高价氧化物对应水化物两两之间都能反应,D为Al元素;结合“D、F、G原子最外层电子数之和等于15”,则F为P元素,G为Cl元素,E为Si元素。
(1)E为Si元素,Si原子核外有3个电子层,最外层电子数为4,E元素在元素周期表中的位置是第三周期IVA族。A离子为O2-,A离子的结构示意图为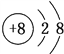 。
。
(2)B的最高价氧化物对应水化物为NaOH,Al与NaOH溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
(3)B2A2为Na2O2。
① Na2O2的电子式为![]() ,Na2O2中含有离子键和非极性共价键。
,Na2O2中含有离子键和非极性共价键。
②Na2O2与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑。
(4)①根据同周期从左到右主族元素的原子半径依次减小,B、D、E原子半径依次减小,①正确;②A元素为O,O没有最高正化合价,②错误;③D的最高价氧化物对应水化物为Al(OH)3,Al(OH)3不溶于氨水,③错误;④非金属性:Cl(G)![]() P(F),气态氢化物稳定性HCl
P(F),气态氢化物稳定性HCl![]() PH3,非金属性:O(A)
PH3,非金属性:O(A)![]() P(F),气态氢化物稳定性H2O
P(F),气态氢化物稳定性H2O![]() PH3,④错误;正确的是①,答案选①。
PH3,④错误;正确的是①,答案选①。
(5)E、F、G依次为Si、P、Cl,根据同周期从左到右非金属元素的最高价氧化物对应水化物酸性逐渐增强,酸性最强的为HClO4。用原子结构解释原因:同周期元素电子层数相同,从左到右,核电荷数依次增大,原子半径逐渐减小,得电子能力逐渐增强,元素非金属性逐渐增强。


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其中pH与溶液体积V的关系如图所示.下列说法正确的是( )
A.A,B两酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强
C.a=5时,A是强酸,B是弱酸
D.若a小于5,则A,B都是弱酸,且A的酸性弱于B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与环境、材料、信息、能源关系密切,下列说法正确的是( )
A.碳纳米管表面积大,可用作新型储氢材料
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.CuSO4因具有氧化性,故用其制成的波尔多液可作“杀菌剂”
D.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2在Cl2中燃烧的方程式为:H2 + Cl2 ![]() 2HCl,已知在相同条件下,有下图所示的能量变化,下列说法中正确的是
2HCl,已知在相同条件下,有下图所示的能量变化,下列说法中正确的是
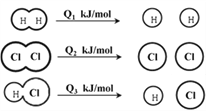
A. H2、Cl2和HCl分子中的化学键都是非极性共价键
B. 1 mol H2与1 mol Cl2的总能量小于2 mol HCl的总能量
C. 1molH2与1molCl2反应生成2 mol HCl时,反应放出的能量为:2Q3-Q1 -Q2
D. 1molH2与1molCl2反应生成2 mol HCl的过程中:Q1+ Q2 >2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明的妈妈在超市购买了面粉、牛肉、桔子和梅子蜜饯,要求小明根据所学知识说出每种食品中所含的一类营养物质.下面是小明的回答,其中错误的是( )
A.面粉﹣淀粉
B.牛肉﹣蛋白质
C.桔子﹣维生素
D.梅子蜜饯﹣防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于药物的说法正确的是( )
A.药物的服用剂量越大,治疗效果越明显
B.包装上印有“OTC“标志的药品属于处方药
C.氢氧化铝可作为抑酸剂,用于治疗胃酸过多
D.长期大量服用阿司匹林可预防某些疾病,没有副作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式或离子方程式正确的是( )
A.苯酚钠溶液中通入少量CO2:2C6H5O﹣+CO2+H2O→2C6H5OH+CO32﹣
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH﹣ ![]() HCOO﹣+NH4++2Ag↓+3NH3+H2O
HCOO﹣+NH4++2Ag↓+3NH3+H2O
C.1一氯丙烷中加入氢氧化钠溶液并加热:CH3CH2CH2Cl+NaOH ![]() CH3CH=CH2↑+NaCl+H2O
CH3CH=CH2↑+NaCl+H2O
D.向小苏打溶液中加入醋酸:HCO3﹣+CH3COOH═CO2↑+H2O+CH3COO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期主族元素Q、T、U、V、W、X、Y、Z原子序数依次增大。已知:T与U、V同周期,W与X、Y、Z同周期,U和Y同族;元素Q的某种核素没有中子;元素T的最高正价与最低负价的代数和为0;Q与U形成的气态化合物在标准状况下的密度为0.76g/L;工业上通过分离液态空气获得V的单质,且该单质的某种同素异形体是保护地球地表环境的重要屏障;W、X、Z的最高价氧化物对应的水化物两两之间都能反应,且W、X、Z原子最外层电子数之和等于W的原子序数。
(1)V元素原子的 L层电子数为______。元素 W 在周期表中的位置为______。
(2)用电子式表示化合物 QZ的形成过程______。
(3)U的氢化物比同主族其他元素的氢化物的熔沸点明显偏高,原因是______。
(4)写出X、Z 两种元素最高价氧化物对应的水化物相互反应的离子方程式:______。
(5)T、U、V形成的氢化物分子中共价键的极性由强到弱的顺序为______。(填化学式)
(6)Q与T可形成一种化合物T2Q4,请写出该分子的结构式________。
(7)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为: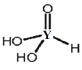 。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式______。(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式______。(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应:2HI(g) ![]() H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
A.HI、H2、I2的浓度相等
B.HI、H2、I2的浓度不再发生变化
C.HI、H2、I2在密闭容器中共存
D.容器内气体的颜色不再发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com