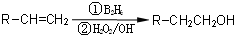分析:(1)根据实验目的,②为制取二氧化碳装置,实验室中常用碳酸钙与盐酸反应,二氧化碳中混有氯化氢,需要用装置④除去,然后用装置③干燥,然后在①中进行钠与二氧化碳的反应,然后用⑤检验反应产物,据此进行连接装置;
(2)所选试剂的作用是增大溶液体积,可以用稀硝酸和硝酸钠溶液,由于四氯化碳的密度大于盐酸,也可以加入四氯化碳溶液,但是苯的密度小于盐酸,加入苯不能使稀盐酸与碳酸钙接触;
(3)二氧化碳与澄清石灰水反应生成碳酸钙沉淀,当装置⑤中澄清石灰水变浑浊说明装置中空气已经排净;原因是空气中的二氧化碳、水与钠反应,需要排净空气,避免干扰实验;
(4)Ⅰ.根据题干信息及反应现象判断反应物、生成物,然后写出反应的化学方程式;
Ⅱ.根据n=
计算出钠的物质的量,再根据n=
计算出标况下224mL二氧化碳的物质的量,从而得出反应后生成碳酸钠的物质的量;溶液中还有固体残留,该固体只能为C,说明钠与二氧化碳反应生成碳酸钠和C,据此写出反应的化学方程式.
解答:
解:(1)探究钠与CO
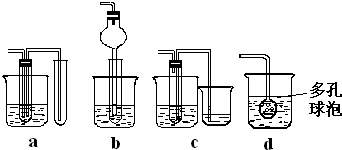
2的反应,首先用盐酸和碳酸钙在②中反应制取二氧化碳气体,制取的二氧化碳中混有挥发出来的HCl,需要用装置④中的饱和碳酸氢钠溶液除去HCl,然后用③浓硫酸干燥,再在①中进行钠与二氧化碳的反应,最后用装置⑤检验反应产物,所以装置的连接顺序为:g、d、e、a(b)、b(a)、h,
故答案为:g、d、e、a(b)、b(a)、h;
(2)A.NaNO
3溶液:加入硝酸钠溶液后,增大了盐酸的体积,可以使盐酸与碳酸钙接触,故A正确;
B.CCl
4:四氯化碳的密度大于稀盐酸,加入四氯化碳后会,四氯化碳层在混合液下层,从而使盐酸与碳酸钙接触,故B正确;
C.苯:苯的密度小于盐酸,加入苯后,苯在混合液上层,无法使稀盐酸与碳酸钙接触,故C错误;
D.稀硝酸:加入稀硝酸后,可以增大溶液体积,使溶液与碳酸钙接触,故D正确;
故答案为:ABD;
(3)钠化学性质比较活泼,能够与空气中的氧气、水反应,所以点燃酒精灯之前应需要打开弹簧夹,让CO
2充满整个装置,以便排尽装置中的空气,避免空气中O
2、H
2O干扰实验;当装置装置⑤中澄清石灰水变浑浊时,证明装置中空气已经排净,
故答案为:装置⑤中澄清石灰水变浑浊;排尽装置中的空气,以免空气中O
2、H
2O干扰实验;
(4)Ⅰ.装置⑤PdCl
2溶液中观察到有黑色沉淀,PdCl
2能被CO还原得到黑色的Pd,则黑色沉淀为Pd,钠与二氧化碳反应生成了CO;装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,该气体为二氧化碳,则钠与二氧化碳反应生成碳酸钠和CO,2Na+2CO
2Na
2CO
3+CO,
故答案为:2Na+2CO
2Na
2CO
3+CO;
Ⅱ.装置①中钠的质量为0.46g,钠的物质的量为:n(Na)=
=0.02mol,
将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO
2气体,二氧化碳的物质的量为:n(CO
2)=
=0.01mol,则反应后生成碳酸钠的物质的量为0.01mol,说明钠完全转化成了碳酸钠;
溶液中还有固体残留,根据化合价变化可知,残留的固体只能为C,则钠与二氧化碳反应生成了碳酸钠和C,反应的化学方程式为:4Na+3CO
22Na
2CO
3+C,
故答案为:4Na+3CO
22Na
2CO
3+C.




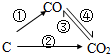 由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.
由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.
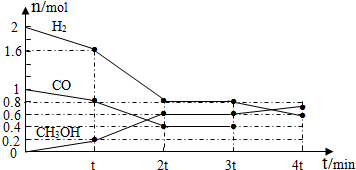
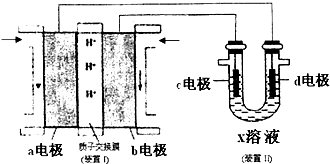

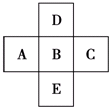 如图所示,已知A元素的最低化合价为-3价,D元素和B元素可形成2种化合物.试回答下列问题(均用具体的元素符号回答):
如图所示,已知A元素的最低化合价为-3价,D元素和B元素可形成2种化合物.试回答下列问题(均用具体的元素符号回答):