

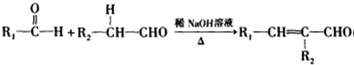 (R1、R2为烃基或氢原子);
(R1、R2为烃基或氢原子); (R1、R2为烃基)
(R1、R2为烃基)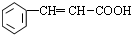 ,逆推可知B为
,逆推可知B为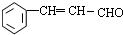 ,结合信息I可知A为
,结合信息I可知A为 .E的核磁共振氢谱图中只有一个吸收峰,则E为(CH3)3CCl,E发生消去反应生成F为CH2=C(CH3)2,F与溴发生加成反应生成G为
.E的核磁共振氢谱图中只有一个吸收峰,则E为(CH3)3CCl,E发生消去反应生成F为CH2=C(CH3)2,F与溴发生加成反应生成G为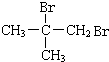 ,G发生水解反应生成H为
,G发生水解反应生成H为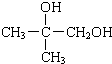 ,H发生催化氧化生成I为
,H发生催化氧化生成I为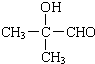 ,I与银氨溶液反应生成J为
,I与银氨溶液反应生成J为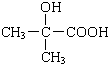 ,J与D发生信息Ⅱ中反应生成K为
,J与D发生信息Ⅱ中反应生成K为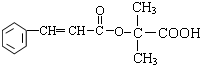 ,据此解答.
,据此解答.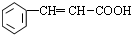 ,逆推可知B为
,逆推可知B为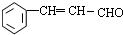 ,结合信息I可知A为
,结合信息I可知A为 .E的核磁共振氢谱图中只有一个吸收峰,则E为(CH3)3CCl,E发生消去反应生成F为CH2=C(CH3)2,F与溴发生加成反应生成G为
.E的核磁共振氢谱图中只有一个吸收峰,则E为(CH3)3CCl,E发生消去反应生成F为CH2=C(CH3)2,F与溴发生加成反应生成G为 ,G发生水解反应生成H为
,G发生水解反应生成H为 ,H发生催化氧化生成I为
,H发生催化氧化生成I为 ,I与银氨溶液反应生成J为
,I与银氨溶液反应生成J为 ,J与D发生信息Ⅱ中反应生成K为
,J与D发生信息Ⅱ中反应生成K为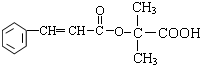 ,
, ,分子式为C7H6O,C→D的反应类型为取代反应,故答案为:C7H6O;取代反应;
,分子式为C7H6O,C→D的反应类型为取代反应,故答案为:C7H6O;取代反应;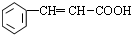 )的同分异构体:能使溶液显紫色,含有酚羟基;能发生银镜反应,含有醛基,能与溴水发生加成反应,则还含有碳碳双键,而苯环上有三个取代基,则为-OH、-CH=CH2、-CHO,-OH与-CH=CH2有邻、间、对三种物质,对应的-CHO分别有4种、4种、2种位置,故共有4+4+2=10种,故答案为:10;
)的同分异构体:能使溶液显紫色,含有酚羟基;能发生银镜反应,含有醛基,能与溴水发生加成反应,则还含有碳碳双键,而苯环上有三个取代基,则为-OH、-CH=CH2、-CHO,-OH与-CH=CH2有邻、间、对三种物质,对应的-CHO分别有4种、4种、2种位置,故共有4+4+2=10种,故答案为:10; ,含有羧基、羟基,在一定条件下可以发生缩聚反应得到一种高聚物,该高聚物的结构简式为
,含有羧基、羟基,在一定条件下可以发生缩聚反应得到一种高聚物,该高聚物的结构简式为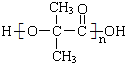 ,故答案为:
,故答案为: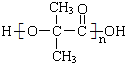 ;
;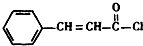 +
+
| 一定条件 |
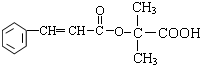 +HCl,
+HCl,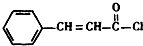 +
+
| 一定条件 |
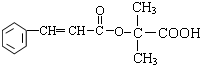 +HCl.
+HCl.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
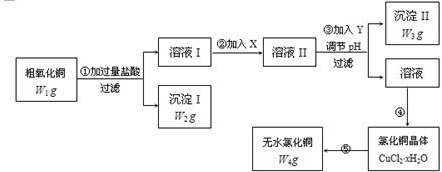
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测液体积(mL) | 标准酸液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 |
| B、用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 |
| C、用碱式滴定管取10.00 mL NaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定 |
| D、用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:| 实验 编号 | NaOH溶液的 浓度/mol?L-1 | 滴定完成时,溶液滴入的体积/mL aOH | 待测盐的体积/mL酸 |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
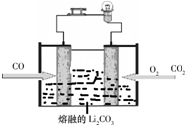 定”).
定”).查看答案和解析>>
科目:高中化学 来源: 题型:
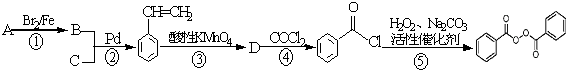
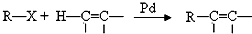
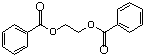 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.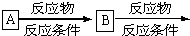
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com