
(12分)烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)3·Al2O3]溶液,并用于烟气脱硫研究。

(1)酸浸时反应的化学方程式为;滤渣I的主要成分为(填化学式)。
(2)滤渣Ⅱ的主要成分为(填化学式);制备碱式硫酸铝[Al2(SO4)3·Al2O3]溶液的化学方程式为 。
(3)吸收烟气中SO2的化学方程式为Al2(SO4)3·Al2O3+3SO2 = Al(SO4)3·Al2(SO3)3。通入空气氧化,发生反应的化学方程式为 ;氧化后循环利用的溶液的pH将 (填“增大”、“减小”或“不变”)。
(1)Al2O3+3H2SO4=Al2(SO4)3+3H2O;SiO2;
(2)CaSO4·2H2O或CaSO4;2 Al2(SO4)3+3CaCO3+6H2O= Al2(SO4)3·Al2O3+3CaSO4·2H2O+CO2↑:
或2Al2(SO4)3+3 CaSO4= Al2(SO4)3·Al2O3+3CaSO4+CO2↑;
(3)2 Al2(SO4)3·2Al2(SO3)3+3O2= 4Al2(SO4)3或2Al2(SO3)3+3O2= 2Al2(SO4)3;减小;
【解析】
试题分析:(1)酸浸时含Al2O3与硫酸发生复分解反应,反应的化学方程式为Al2O3+3H2SO4=Al2(SO4)3+3H2O;SiO2等不能与酸反应,所以滤渣I的主要成分是SiO2;(2)在滤液中含有过量的硫酸和硫酸铝,当向其中加入CaCO3时,会发生复分解反应:CaCO3+H2SO4= CaSO3+ CO2↑+ H2O;由于硫酸钙微溶于水,所以滤渣Ⅱ的主要成分为CaSO4或写为石膏CaSO4·2H2O;制备碱式硫酸铝[Al2(SO4)3·Al2O3]溶液的化学方程式为2Al2(SO4)3+3CaCO3+6H2O= Al2(SO4)3·Al2O3+3CaSO4·2H2O+CO2↑: 或2Al2(SO4)3+3 CaSO4= Al2(SO4)3·Al2O3+3CaSO4+CO2↑;(3)吸收烟气中SO2的化学方程式为Al2(SO4)3·Al2O3+3SO2 = Al(SO4)3·Al2(SO3)3。通入空气氧化,空气中的氧气能够把Al2(SO3)3氧化为Al(SO4)3·发生反应的化学方程式为2 Al2(SO4)3·2Al2(SO3)3+3O2= 4Al2(SO4)3或2Al2(SO3)3+3O2= 2Al2(SO4)3;氧化后循环利用的溶液由弱酸弱碱盐变为强酸弱碱盐,所以溶液的酸性增强,故溶液的pH将减小。
考点:考查物质的性质及转化的方程式表示、盐的水解的知识。


科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:选择题
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是
编号 | ① | ② | ③ | ④ |
气体M | H2S | H2 | NH3 | NO |
气体N | SO2 | Cl2 | HCl | O2 |
A.①②③④ B.①④③② C.②④①③ D.④①②③
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA
B.1L 1mol·L-1的NaClO 溶液中含有ClO-的数目为NA
C.质量a g的C2H4和C3H6的混合物中共用电子对数目为3a NA /14
D.常温下,pH=13的NaOH溶液中含有OH一的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届江西五校高三第一次联考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是( )
A.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+ 6H+ =2Mn2+ + 5NO3- + 3H2O
B.碳酸氢铵溶液中加入足量氢氧化钡溶液: NH4++HCO3-+2OH-=CO32-+ NH3?H2O +H2O
C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ + 2I- =2Fe 2+ + I2
D.用惰性电极电解熔融氯化钠: 2Cl—+2H2O=Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:填空题
(12分)已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如下图:
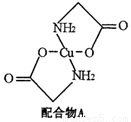
(1)Cu元素基态原子的外围电子排布式为。
(2)元素C、N、O的第一电离能由大到小排列顺序为。
(3)配合物A中碳原子的轨道杂化类型为。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有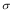 键的数目为。
键的数目为。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:(写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图,
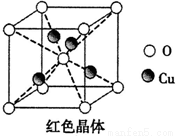
则该化合物的化学式是。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3
B.反应Hg(1)+H2SO4(aq) = HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0
C.将纯水加热至较高温度,K变大、pH变小、呈酸性
D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列物质性质与应用对应关系正确的是
A.漂白粉在空气中不稳定,可用于漂白纸张
B.医用酒精能使蛋白质变性,可用于消毒杀菌
C.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
D.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
在容积相同的A、B两个密闭容器中,分别充入2molSO2和1molO2,使它们在相同温度下发生反应:2SO2+O2 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
A.25% B.>25% C.<25% D.12.5%
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:填空题
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
CO2(g)+H2(g) ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
起始物质的量 | 甲 | 乙 | 丙 |
n(H2O)/mol | 0.10 | 0.20 | 0.20 |
n(CO)/mol | 0.10 | 0.10 | 0.20 |
(1)该反应的平衡常数表达式为 。
(2)平衡时,甲容器中CO的转化率是 。比较下列容器中CO的转化率:乙 甲;丙 甲(填“>”、“=”或“<”)。
(3)丙容器中,若要通过改变温度,使CO的平衡转化率增大,则温度需要降低才能达到,则降温后的平衡常数K (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com