
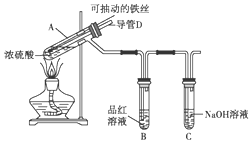
分析 浓硫酸和Fe在加热条件下发生氧化还原反应生成硫酸Fe、二氧化硫和水,Fe能和硫酸铁反应生成硫酸亚铁,当浓硫酸达到一定浓度后变为稀硫酸,Fe和稀硫酸反应生成硫酸亚铁和氢气,二氧化硫能使品红溶液褪色,所以看到B中溶液褪色,二氧化硫为酸性氧化物,能被碱性溶液吸收,所以C的作用是吸收二氧化硫;
(1)实验过程中,观察到B中的品红溶液褪色,C中二氧化硫和NaOH溶液反应生成亚硫酸钠和水;二氧化硫能和NaOH反应但氢气不反应;
(2)用“可抽动的铁丝”代替“直接投人铁片”可以控制反应速率;
(3)A中气体和外界相通,能利用大气压平衡A中压强;
(4)SO2有毒,为防止SO2污染空气,应该将装置中气体全部通入NaOH溶液中,使SO2被完全吸收;
(5)亚铁离子能和铁氰化钾反应生成特征蓝色沉淀,也能将酸性高锰酸钾溶液还原而使酸性高锰酸钾溶液褪色;
(6)酸性溶液应该盛放在酸式滴定管中,若滴定前滴定管中有气泡,滴定后气泡消失,会导致标准液体积偏大.
解答 解:浓硫酸和Fe在加热条件下发生氧化还原反应生成硫酸Fe、二氧化硫和水,Fe能和硫酸铁反应生成硫酸亚铁,当浓硫酸达到一定浓度后变为稀硫酸,Fe和稀硫酸反应生成硫酸亚铁和氢气,二氧化硫能使品红溶液褪色,所以看到B中溶液褪色,二氧化硫为酸性氧化物,能被碱性溶液吸收,所以C的作用是吸收二氧化硫;
(1)二氧化硫有毒,需要用氢氧化钠溶液吸收,二者反应生成亚硫酸钠和水,反应的离子方程式为:SO2+2OH-═SO32-+H2O;
A中开始可能发生的反应有:2Fe+6H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O、Fe+Fe2(SO4)3=3FeSO4,随着反应的进行,浓硫酸变为稀硫酸,铁与稀硫酸反应产生氢气,氢气不和NaOH反应,所以C中逸出的气体是H2;
故答案为:SO2+2OH-═SO32-+H2O;H2;
(2)将抽动的铁丝脱离液面,反应停止,将抽动的铁丝插入液面,反应开始,
故答案为:便于控制铁与浓硫酸的反应和停止;
(3)当A中气体压强减小时,外界大气压不变,空气从E进入A,使A中压强平衡,所以B中压强不会产生倒吸,
故答案为:当A中气体压强减小时,外界大气压不变,空气从E进入A,使A中压强平衡;
(4)SO2有毒不能直接排空,为防止SO2污染空气,应该将装置中气体全部通入NaOH溶液中,使SO2被完全吸收,其基本操作方法为从E管口向A中缓缓鼓入足量空气,将残留的二氧化硫赶入NaOH溶液中,使其完全被吸收,
故答案为:从E管口向A中缓缓鼓入足量空气,将残留的二氧化硫赶入NaOH溶液中,使其完全被吸收;
(5)亚铁离子能和铁氰化钾反应生成特征蓝色沉淀,也能将酸性高锰酸钾溶液还原而使酸性高锰酸钾溶液褪色,铁离子和铁氰化钾及酸性高锰酸钾溶液都不反应,所以可以选取铁氰化钾或酸性高锰酸钾溶液检验亚铁离子,
故答案为:BD;
(6)酸性溶液应该盛放在酸式滴定管中,酸性高锰酸钾溶液具有酸性,应该盛放在酸式滴定管中;若滴定前滴定管中有气泡,滴定后气泡消失,会导致标准液体积偏大,则测定结果偏高,
故答案为:酸;偏高.
点评 本题以浓硫酸和Cu反应为载体考查性质实验方案设计,题目难度中等,明确实验原理是解本题关键,侧重考查学生实验操作、分析能力,知道各个装置目的、作用、发生的反应及实验现象,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 能被银氨溶液氧化 | |
| B. | 能使KMnO4酸性溶液褪色 | |
| C. | 1mol该有机物只能与1molBr2发生加成反应 | |
| D. | 1mol该有机物只能与1molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑧ | B. | ①⑥ | C. | ②④ | D. | ③⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 均减半 | B. | 均加倍 | C. | 均减少1mol | D. | 均增加1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为1NA | |
| B. | 常温常压下,7.1g Cl2与足量的Fe充分反应,转移的电子数目为0.3 NA | |
| C. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,1L溶液中含有Cl-个数为1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3+CaCl2═CaCO3↓+2NaCl | B. | Fe+CuSO4═Cu+FeSO4 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | NaOH+HCl═NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 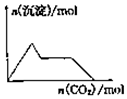 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 | |
| B. | 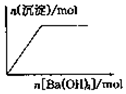 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 | |
| C. | 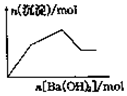 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 | |
| D. | 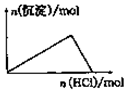 向NaAlO2溶液中逐滴加入盐酸至过量 |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,其中电极I为Al,其它均为Cu,下列说法正确的是( )

A.装Al2(SO4)3 溶液的烧杯是原电池,其余两个为电解(电镀)池
B.盐桥中电子从右侧流向左侧
C.电极II逐渐溶解
D.电极IV的电极反应:Cu2+ + 2e- = Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com