
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。

(1)酸浸时发生的反应的离子方程式为 ▲ ;为提高BaCO3的酸浸率,可采取的措施为 ▲ (任答一点)。
(2)煅烧草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O]得到BaTiO3的同时,生成高温下的气体产物有CO、 ▲ 和 ▲ 。
(3)加入H2C2O4溶液时,发生反应的化学方程式为 ▲ ;
可循环使用的物质X是 ▲ 。
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是
| A | B高考在线 | C | D高考在线 | |
| 装置 |
|
|
|
|
| 实验 | 干燥氯气高考在线 | 吸收NH3 w.&w.^w.k.s.5*u.c.#o@ | 石油的分馏 | 制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
条件一定时,反应2A(g)+B(g) 2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V(正)<V(逆)的点是
2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V(正)<V(逆)的点是
A. a B. b C. c D. d

查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是:CO(g)+2H2(g)  CH3OH(g) △H=-90.8 kJ/mol ①
CH3OH(g) △H=-90.8 kJ/mol ①
已知:2H2(g)+ O2(g)= 2H2O (l) △H=-571.6 kJ/mol ②
H2(g) + O2(g) = H2O(g) △H=-241.8 kJ/mol ③
O2(g) = H2O(g) △H=-241.8 kJ/mol ③
①H2的燃烧热为 ▲ kJ/mol。
②CH3OH(g)+O2(g)  CO(g)+2H2O(g)的反应热△H= ▲ kJ/mol。
CO(g)+2H2O(g)的反应热△H= ▲ kJ/mol。
③若在恒温恒容的容器内进行反应CO(g)+2H2(g)  CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
A.CO百分含量保持不变 B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变 D.H2的生成速率与CH3OH的生成速率相等
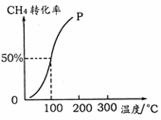 (2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为 ▲ 。
②100℃时反应I的平衡常数为 ▲ 。
(3)工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸汽重整法。该法中的一个主要反应为CH3OH(g)  CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
②甲醇部分氧化法。在一定温度下以Ag/CeO2—ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图所示。

则当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应方程式为
▲ ;
在制备H2时最好控制n(O2)/n(CH3OH)= ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
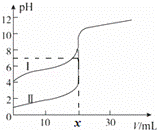
室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )
|
| A. | I曲线表示的是滴定盐酸的曲线 |
|
| B. | x=20 |
|
| C. | 滴定过程中 |
|
| D. | 当I曲线和II曲线pH均为7时,一溶液中的c(Cl﹣)等于另一溶液中的c(CH3COO﹣) |
查看答案和解析>>
科目:高中化学 来源: 题型:
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极。则四种金属的活动性顺序由大到小排列为 ( )
A.A>B>C>D B.A>C>B>D C.A>C>D>B D.B>D>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
1mol某气态烃最多可与2mol的HCl发生加成反应,所得产物与Cl2发生取代反应,若将氢原子全部取代,需要8mol的Cl2,则该烃的结构简式可能为
A. B.
B.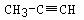 C.
C.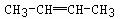 D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com