
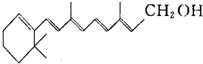
 维生素A的结构简式如图所示,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来.关于它的叙述正确的是( )
维生素A的结构简式如图所示,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来.关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H28O | |
| B. | 维生素A是一种易溶于水的醇 | |
| C. | 维生素A能与酸发生酯化反应 | |
| D. | 1 mol维生素A在催化剂作用下最多可与7 mol H2发生加成反应 |
分析 A.根据结构简式确定分子式;
B.该物质中含有醇羟基,但亲水基对物质溶解性的影响远远小于憎水基;
C.醇在一定条件下能和羧酸发生酯化反应;
D.碳碳双键能和氢气在一定条件下发生加成反应.
解答 解:A.根据结构简式确定分子式C20H30O,故A错误;
B.烃基较大,不易溶于水,故B错误;
C.醇在一定条件下能和羧酸发生酯化反应,该物质中含有醇羟基,所以能和羧酸在一定条件下发生酯化反应,故C正确;
D.含5个双键,1mol维生素A 在催化剂作用下最多可与5molH2发生加成反应,故D错误;
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,答题时注意把握有机物的结构特点和官能团的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14 g丙烯和丁烯的混合气体含有的原子数为6NA | |
| B. | 25℃,pH=1的1 L H2SO4溶液含有的H+数目为0.2NA | |
| C. | 1 mol Fe与一定量的HNO3反应,转移的电子数目一定为3NA | |
| D. | 标准状况下,22.4 L NO和O2的混合气体中所含原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①②④ | C. | ②③ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X、Y、Z三种元素的最简单氢化物中最不稳定的是Y | |
| B. | W、Y、Z三种元素对应氧化物的水化物一定都是强酸 | |
| C. | W、X元素的最简单氢化物都是非电解质 | |
| D. | Z元素的单质在化学反应中只能表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| T | M层电子数是K层电子数的3倍 |
| X | 一种同位素可测定文物年代 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Sn(NO3)4 | B. | Sn(NO3)2 | C. | SnO2?4H2O | D. | SnO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨是重要的化工原料,用途广泛.
氨是重要的化工原料,用途广泛.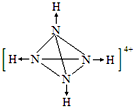 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com