
分析 硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO•nSiO2•mH2O).注意:①氧化物之间以“•”隔开;②系数配置出现的分数应化为整数;③金属氧化物在前(活泼金属氧化物→较活泼金属氧化物),非金属氧化物在后,若同一元素有变价,那么低价在前,高价在后,H2O一般写在最后.
解答 (1)硅酸盐改写成氧化物的形式为:活泼金属氧化物•较活泼金属氧化物•SiO2•H2O,同时要遵循原子守恒,普通玻璃中Na2CaSi6O14,以氧化物的形式表示故写成Na2O•CaO•6SiO2,
故答案为:Na2O•CaO•6SiO2.
普通玻璃的成分Na2CaSi6O14,
(2)Na2O•CaO•6SiO2的摩尔质量为478g/mol,7.17吨Na2O•CaO•6SiO2的物质的量为:$\frac{7.17×1{0}^{6}g}{478g/mol}$=1.5×104mol,
设需要石灰石、石英的质量分别为x、y,
则:75%x=1.5×104mol×100g/mol,解得:x=2×106g=2吨;
75%y=60g/mol×1.5×104mol,解得:y=1.2×106g=1.2吨;
根据质量守恒可知:n(CO2)=$\frac{1}{2}$n(Na2CO3)+n(CaCO3)=1.5×104mol×2×$\frac{1}{2}$+1.5×104mol=3×104mol,标况下3×104mol二氧化碳气体的体积为:22.4L/mol×3×104mol=672×103L=672立方米
答:石灰石:2吨;石英:1.2吨; CO2:672立方米.
点评 本题考查硅酸盐的性质和硅酸盐改写为氧化物的形式的方法,题目难度不大,注意硅酸盐改写为氧化物的一般方法为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO•nSiO2•mH2O).


科目:高中化学 来源: 题型:选择题
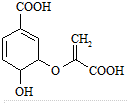
| A. | 分枝酸分子中含有2种官能团 | |
| B. | 分枝酸可与乙醇发生酯化反应 | |
| C. | 分枝酸是芳香族化合物 | |
| D. | 1mol分枝酸最多可与3molNaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 被鉴别的物质 | 鉴别物质(或鉴别方法) | 现象(填入序号即可) |
| 葡萄糖 | 新制氢氧化铜 | ④ |
| 淀粉 | 碘水 | ② |
| 蛋白质 | 浓硝酸 | ⑤ |
| 蛋白质 | 燃烧 | ① |
| 葡萄糖 | 银氨溶液 | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
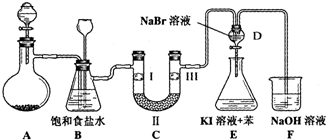
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积:④>①>②>③ | B. | 密度:②>③>①>④ | ||
| C. | 质量:②>③>①>④ | D. | 氢原子数:①>②>③>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度 | B. | 混合气体的压强 | ||
| C. | 混合气体的平均摩尔质量 | D. | SO2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
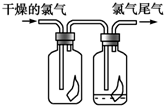 (1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com