
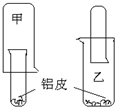
 为了适应“低碳生活”,某化学兴趣小组用铝制废牙膏皮、一大一小两种试管和稀硫酸来制取并收集一试管氢气.据此完成下列要求.
为了适应“低碳生活”,某化学兴趣小组用铝制废牙膏皮、一大一小两种试管和稀硫酸来制取并收集一试管氢气.据此完成下列要求.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
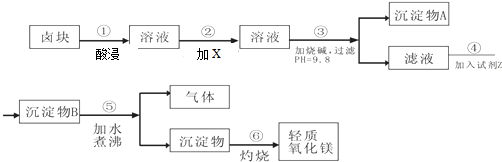
名师指导一卷通系列答案科目:高中化学 来源: 题型:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 试剂 | 价格(元/吨) |
| 漂液(含NaClO,25.2%) | 450 |
| 双氧水(含H2O2,30%) | 2400 |
| 烧碱(含98% NaOH) | 2100 |
| 纯碱(含99.5% Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管 | 未加MnSO4的试管 | 加有MnSO4的试管 |
| 褪色时间 | 30s | 2s |
| 试管 | 未滴加稀硫酸的试管 | 滴加了稀硫酸的试管 |
| 褪色时间 | 100s | 90s |
| 试管 | 滴入10滴稀硫酸的试管 | 加入1mL稀硫酸的试管 | 加入2mL稀硫酸的试管 |
| 褪色时间 | 70s | 100s | 120s |
| Mn2+ |
| Mn2+ |
| Mn2+ |
| C2O42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验现象 | 结论 | |
| 实验① | ||
| 实验② |
查看答案和解析>>
科目:高中化学 来源: 题型:
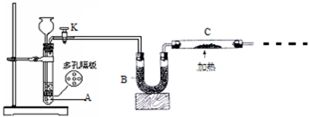 某化学课外活动小组拟用Zn和稀H2SO4制取H2还原CuO,实验装置如图.
某化学课外活动小组拟用Zn和稀H2SO4制取H2还原CuO,实验装置如图.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成氨工业中,将NH3及时液化分离有利于加快反应速率 |
| B、硫酸工业中,接触室内安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C、氯碱工业中,使用离子交换膜可防止C12和NaOH溶液反应 |
| D、电镀工业中,必需将镀件与电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| △ |
| HCl |
| △ |
| NH3 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
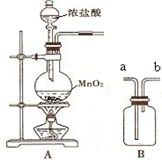 实验室用如图所示装置A、B进行组合制取氯气,按要求回答下列问题:
实验室用如图所示装置A、B进行组合制取氯气,按要求回答下列问题:| 实验目标 | 装填试剂 (填选项字母) | 气体流向 (填a、b) |
| 除去HCl杂质 | E | a→b |
| 干燥氯气 | C | a→b |
| 收集氯气 | D | |
| 检验氯气的氧化性 | F |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com