
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)A、B两仪器的名称:A________,B________。
(2)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C、D中应分别放入C_______;D________
①NaOH溶液 ②饱和食盐水 ③AgNO3溶液 ④浓H2SO4
(3)E中为红色干布条,F中为红色湿布条,可观察到______________________________。
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成____________。反应的离子方程式是_______,H是浸有NaBr溶液的棉花球,H处现象是棉花球表面变________。
(5)P处为尾气吸收装置,可选用____________________。

【答案】(1)分液漏斗;圆底烧瓶;(2)②;④;(3)E中无变化,F中为红色布条褪色;(4)蓝色;Cl2+2I-===I2+2Cl- ;橙色;(5)D。
【解析】
试题(1)通过对实验装置图进行观察,可确定A是分液漏斗;B是圆底烧瓶;(2)在实验室中用浓盐酸与MnO2混合加热制取Cl2,由于浓盐酸具有挥发性,实验洗气装置C是为了除去Cl2中的HCl气体,其中盛有的试剂是饱和食盐水,D是为了干燥Cl2,由于氯气是酸性气体,实验D装置盛有的试剂是浓硫酸;故试剂序号分别是②;④;(3)E中为红色干布条,F中为红色湿布条,可观察到E中无变化,F中为红色布条褪色;说明SO2的漂白性在溶液中才可以表现出来;(4)G是浸有淀粉KI溶液的棉花球,Cl2与KI发生反应:Cl2+2KI=2KCl+I2,I2遇淀粉溶液变为蓝色,实验G处现象是棉花球表面变成蓝色.反应的离子方程式是Cl2+2I-=I2+2Cl- ;H是浸有NaBr溶液的棉花球,Cl2与NaBr发生反应:Cl2+2NaBr===2NaCl+Br2 ,H处现象是棉花球表面变成橙色;(5)Cl2是有毒的气体,要进行尾气处理,由于该物质可与碱发生反应,实验P处为尾气吸收装置,可选用NaOH溶液,为防止倒吸现象的发生,所以应该选择D装置。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】钒和镍及其化合物是重要合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的核外电子排布式为________,其排布时能量最高电子所占据能级的原子轨道有________个伸展方向。
(2)VO2+可与多种物质形成配合物,与氧同周期且第一电离能比氧大的主族元素有____(写元素符号)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______,与CN-互为等电子体的一种分子的化学式为__________。
(4)三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF3、H2O2等为主要原料来制取。
①H2O2分子中O原子的杂化方式为________。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为__________。

(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2所示,该晶胞中S2-的配位数为____。
(6)镧镍合金是重要储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为___________。
②该镧镍合金储氢后氢气的密度为________(用NA表示阿伏加德罗常数的数值)g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是()。

A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化为电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后.向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D. 甲池中消耗280mL(标准伏况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A. ①②B. ②③C. ③④D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有 NOx、![]() (PAN)、HCOOH、等二次污染物。
(PAN)、HCOOH、等二次污染物。
① 1mol PAN中含有的σ键数目为_______。PAN中C、N、O种元素的第一电离能由大到小的顺序为_________________。
② NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为________,中心离子的核外电子排布式为_______________。
③相同压强下,HCOOH的沸点比CH3OCH3____(填“高”或“低”),其原因是__________________。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
① (NH4)2SO4晶体中各种微粒间的作用力不涉及___________(填序号)。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
② NH4NO3中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图(甲)所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=_____(填数字)。

(4)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图(乙)所示。已知晶胞参数a=333.7pm,阿伏加德罗常数的值取6.02×1023,则重冰的密度为_______g.cm-3(计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O35H2O在化学定量分析中常用作基准物质,实验室制备原理为Na2S + Na2CO3 + 4SO2 ![]() 3Na2S2O3 + CO2。现设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3 + CO2。现设计如下装置(夹持仪器省略)进行实验。

(1)A中发生反应的化学方程式为_______________________________。
(2)C中所盛试剂可能是_______________;若要停止A中的化学反应,除取下酒精灯加热外,还可以采取的操作是__________________________。
(3)甲同学在加热A后,发现液面下的铜丝变黑。该同学对黑色生成物提出如下假设:
① 可能是CuO; ② 可能是Cu2O; ③ 可能是CuS
乙同学认为假设②一定不成立,依据是__________;该同学设计如下实验进一步验证黑色物质的组成:
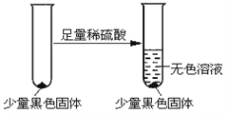
基于上述假设分析,黑色物质的组成为________(填化学式)。
(4)实验室用Na2S2O3标准溶液测定废水中Ba2+ 的浓度,过程如下:(已知:2S2O32-+I2==S4O62-+2I-)。
![]()
① 写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式:________;
② 若以淀粉为指示剂,则达到滴定终点时的现象是__________________。
③ 若Na2S2O3标准溶液的浓度为0.0030 molL-1,消耗该Na2S2O3标准溶液的体积如图所示,则废水中Ba2+ 的浓度为___________。
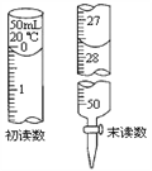
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率的关系是2v逆(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CH3COCH3(1)![]() CH3COCH2COH(CH3)2(1)。取等量CH3COCH分别在0℃和20℃下反应,测得其转化率(α)随时间(t)变化的关系曲线如右图所示。下列说法正确的是
CH3COCH2COH(CH3)2(1)。取等量CH3COCH分别在0℃和20℃下反应,测得其转化率(α)随时间(t)变化的关系曲线如右图所示。下列说法正确的是
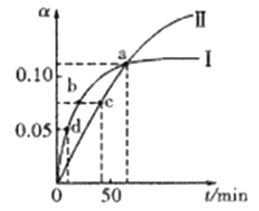
A. 曲线Ⅱ表示20℃时的转化反应
B. 升高温度能提高反应物的平衡转化率
C. 在a点时,曲线Ⅰ和Ⅱ表示反应的化学平衡常数相等
D. 化学反应速率的大小顺序为:d>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com