
| A£®ÓĆÕōĮóĖ®Łž¾»µĪ¶Ø¹Üŗó£¬×°Čė±ź×¼ŃĪĖį½ųŠŠµĪ¶Ø |
| B£®ÓĆÕōĮóĖ®Łž¾»×¶ŠĪĘæŗó£¬ŌŁÓĆNaOHŅŗČóĻ“£¬¶ųŗó×°ČėŅ»¶ØĢå»żµÄNaOHČÜŅŗ |
| C£®ÓĆ¼×»ł³Č×öÖøŹ¾¼Į£¬µ±ČÜŅŗÓÉ»ĘÉ«±ä³É³ČÉ«£¬Į¢æĢ¶ĮŹżŃĪĖįĢå»ż”£ |
| D£®ÓĆ¼īŹ½µĪ¶Ø¹ÜČ”10.00 mLNaOHČÜŅŗ·ÅČėÓĆÕōĮóĖ®Ļ“¾»µÄ׶ŠĪĘæÖŠ£¬ŌŁ¼ÓČėŹŹĮæÕōĮóĖ®½ųŠŠµĪ¶Ø |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®CO32£ | B£®Fe3+ | C£®HSO4£ | D£®Cl£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ¦¤H="-542.7" kJ”¤mol-1 |
| B£®2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ¦¤H="-1059.3" kJ”¤mol-1 |
C£®N2H4(g)+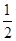 N2O4(g)= N2O4(g)=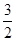 N2(g)+2H2O(g) ¦¤H="-1076.7" kJ”¤mol-1 N2(g)+2H2O(g) ¦¤H="-1076.7" kJ”¤mol-1 |
| D£®2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ¦¤H="-1076.7" kJ”¤mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®1:9 | B£®1:1 | C£®2:9 | D£®1:2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
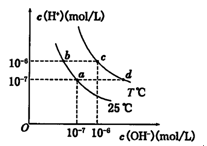
| A£®Ķ¼ÖŠT>25 |
| B£®bµćČÜŅŗc(H+)Ņ»¶Ø±Čaµć“ó |
| C£®cµć¶ŌÓ¦µÄČÜŅŗÖŠæÉÄÜ“óĮæ“ęŌŚAl3+”¢Cl”Ŗ |
| D£®dµć¶ŌÓ¦µÄČÜŅŗ³Ź¼īŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®1”Į10£7mol”¤L£1 | B£®1”Į10£12mol”¤L£1 |
| C£®1”Į10£2mol”¤L£1 | D£®1”Į10£14mol”¤L£1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®Ė®µÄµēĄė³£ŹżKWŹżÖµ“󊔹ŲĻµĪŖ£ŗb£¾c£¾d |
| B£®aµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚ£ŗFe3£«”¢Na£«”¢Cl£”¢SO42- |
| C£®ĪĀ¶Č²»±ä£¬¼ÓČėÉŁĮæNaOHæÉŹ¹ČÜŅŗ“Ócµć±äµ½ aµć |
| D£®ŌŚbµć¶ŌÓ¦ĪĀ¶ČĻĀ£¬½«pH=2µÄHClÓėpH=10µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗĻŌÖŠŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®H2OµÄµē×ÓŹ½ĪŖ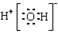 |
| B£®273K”¢101kPa£¬Ė®µÄ·Ö×Ó¼ä¾ąĄė£ŗd£ØĘųĢ¬£©£¾d£ØŅŗĢ¬£©£¾d£Ø¹ĢĢ¬£© |
| C£®4”ꏱ£¬“æĖ®µÄpH=7 |
| D£®D216OÖŠ£¬ÖŹĮæŹżÖ®ŗĶŹĒÖŹ×ÓŹżÖ®ŗĶµÄĮ½±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®x=20 |
| B£®Ļ”H2SO4µÄÅضČĪŖ0.10mol/L |
| C£®bµćÓŠ£ŗ2c(NH4+) = c(SO42-)> c(H+) = c(OH-) |
| D£®aµćÓŠ£ŗc(NH4+) < 2c(SO42-) |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com