
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
将盛有12 mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2 mL 无色气体,则原混合气体中O2的体积是( )
①1.2 mL ②2.4 mL ③3.6 mL ④4 mL
A.①② B.①③
C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误(正确打“√”,错误的打“×”,并改正)
(1)Na2S  ( )
( )
(2)Na2O 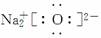 ( )
( )
(3)MgBr2 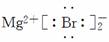 ( )
( )
(4)H2O 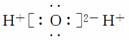 ( )
( )
(5)OH- 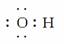 ( )
( )
(6)HClO 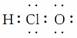 ( )
( )
(7)Cl2 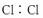 ( )
( )
(8)O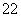
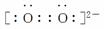 ( )
( )
(9)羟基 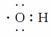 ( )
( )
(10)H2S 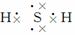 ( )
( )
(11)Na+ 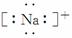 ( )
( )
(12) ( )
( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学键的叙述正确的是( )
A.非金属元素组成的化合物中只含共价键
B.C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键
C.不同元素的原子构成的分子只含极性共价键
D.CH4中所有的价电子都参与形成共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成气态分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同的电子数,且D是同周期元素中原子半径最大的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)X的化学名称为_________________________________________________________。
(2)B单质的结构式为______________________________________________________;
E的气态氢化物的结构式为__________________________________________;
C与D形成的两种化合物中,其中一种物质含有两种类型的化学键,该物质属于________________________________________________________________________
(填“离子化合物”或“共价化合物”)。
(3)B、C、E分别与A形成的化合物中最稳定的是______(写化学式)。
(4)D是同周期简单阳离子中离子半径最____的元素。
(5)F的单质在反应中常作________剂(填“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是几种常见的加热装置。
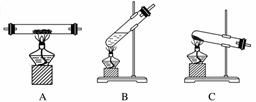

(1)A、B、C、D四装置都是用酒精灯直接加热,E、F装置加热时需垫________________。其中F装置中对试管的加热方式是________________,采用这种加热方式的目的是____________________。
(2)H2还原CuO可选用________装置。
(3)NH4Cl与Ca(OH)2混合加热制NH3可选用______装置。
(4)胆矾中结晶水含量的测定可选用________装置。
(5)乙酸乙酯的制备可选用________装置。
(6)MnO2与浓盐酸混合制氯气可选用________装置。若该装置只加热液体时,容器内必须放________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( )

A.22.30 mL B.22.35 mL
C.23.65 mL D.23.70 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70% Cu、25% Al、4% Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
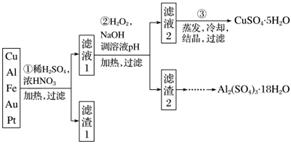
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为____________________________________________
________________________________________________________________________;
得到滤渣1的主要成分为____________。
(2)第②步加H2O2的作用是______________,使用H2O2的优点是______________;调溶液pH的目的是使______________生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是___________________________。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
甲: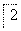
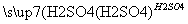
 ,蒸发、冷却、结晶、过滤
,蒸发、冷却、结晶、过滤
Al2(SO4)3·18H2O
乙: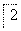
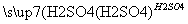

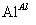

,蒸发、冷却、结晶、过滤Al2(SO4)3·18H2O
丙: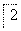
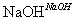

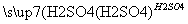

,蒸发、冷却、结晶、过滤Al2(SO4)3·18H2O
上述三种方案中,________方案不可行,原因是________________________________
________________________________________________________________________;
从原子利用率角度考虑,__________方案更合理。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com