
【题目】下列物质属于电解质的是
A. 铝制导线 B. 氨水 C. 稀硫酸 D. 硝酸钠
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】环保、安全的铝--空气电池的工作原理如图所示,下列有关叙述错误的是
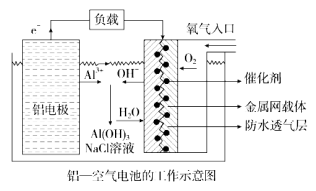
A.电池工作过程中,电解质溶液的pH不断增大
B.正极的电极反应式为O2 + 4e-+ 2H2O =4OH-
C.NaCl的作用是增强溶液的导电性
D.用该电池做电源电解KI溶液制取1 mol KIO3,消耗铝电极的质量为54 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是
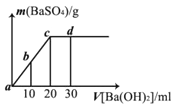
A. 溶液的pH:a<b<c<d
B. 溶液的导电能力:a>b>d>c
C. a、b溶液呈酸性
D. c、d溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+ N(g)![]() xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。
xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。
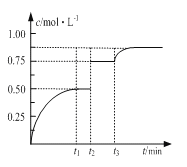
下列说法正确的是
A. 反应方程式中的x=1
B. t2时刻改变的条件是使用催化剂
C. t3时刻改变的条件是移去少量物质Q
D. t1~t3间该反应的平衡常数均为4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 该温度下此反应的平衡常数K =1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如图:
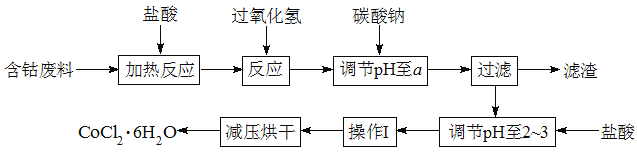
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110 ~120℃时,失去结晶水变成有毒的无水氯化钴。
③物质的熔沸点随压强降低而降低
④乙醚沸点为34.6℃
⑤部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)在上述工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,从环保角度分析其主要优点为_______________________。
(2)加入碳酸钠调节pH至a ,a的范围是____________________________。
(3)操作Ⅰ包含3个实验基本操作,它们依次是_____________、______________和过滤。
(4)制得的CoCl2·6H2O在烘干时需减压烘干的原因是____________________________。
(5)在实验室,为了从上述产品中获得纯净的CoCl2·6H2O,通常先将产品溶解在乙醚中,通过过滤除去不溶性杂质后,再进行_________(填操作名称)。
(6)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是______________。(答出一个原因即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com