
【题目】锌锰干电池所含的汞、酸或碱等在废弃后进入环境中将造成严重危害.对废旧电池进行资源化处理显得非常重要.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源.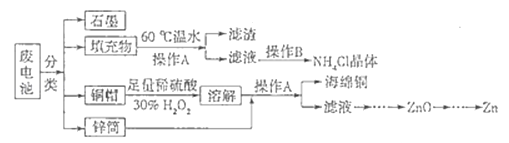
(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2 , 其负极的电极反应式为
(2)填充物用60℃温水溶解,目的是加快溶解速率,但必须控制温度不能太高,其原因是
(3)操作A的名称为
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①当1mol MnO2参加反应时,共有 mol电子发生转移.
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:
(5)铜帽溶解时加入H2O2的目的是 (用化学方程式表示).铜帽溶解完全后,可采用 方法除去溶液中过量的H2O2 .
(6)锌锰干电池所含的汞可用KMnO4溶液吸收.在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图所示:
根据图可知: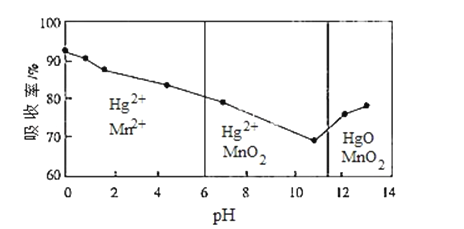
①pH对Hg吸收率的影响规律是
②在强酸性环境下Hg的吸收率高的原因可能是
【答案】Zn+2OHˉ﹣2eˉ=Zn(OH)2;温度过高氯化铵受热分解;过滤;4;2MnO(OH)+6HCl(浓)![]() 2MnCl2+Cl2↑+4H2O;Cu+H2O2+H2SO4=CuSO4+2H2O;加热;着pH的增大,汞的吸收率先减小后增大;高锰酸钾在酸性条件下氧化性强
2MnCl2+Cl2↑+4H2O;Cu+H2O2+H2SO4=CuSO4+2H2O;加热;着pH的增大,汞的吸收率先减小后增大;高锰酸钾在酸性条件下氧化性强
【解析】(1)负极发生氧化反应,由方程式可知Zn被氧化生成Zn(OH)2 , 则电极方程式为Zn+2OHˉ﹣2eˉ=Zn(OH)2 , 故答案为:Zn+2OHˉ﹣2eˉ=Zn(OH)2;
(2)较高温度时,氯化铵易分解生成氯化氢和氨气,所以得不到氯化铵晶体,故答案为:温度过高氯化铵受热分解;
(3)操分离不溶性固体和溶液采用过滤的方法,所以该操作名称是过滤,故答案为:过滤;
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2 MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①该反应中,氧化剂是MnO(OH)、MnO2 , 还原剂是草酸,当1mol MnO2参加反应时,转移电子的物质的量=![]() =4mol,故答案为:4;
=4mol,故答案为:4;
②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水,反应方程式为:2MnO(OH)+6HCl(浓)![]() 2MnCl2+Cl2↑+4H2O,
2MnCl2+Cl2↑+4H2O,
故答案为:2MnO(OH)+6HCl(浓)![]() 2MnCl2+Cl2↑+4H2O;
2MnCl2+Cl2↑+4H2O;
(5)酸性条件下,双氧水能将铜氧化生成铜离子反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;加热条件下,双氧水易分解生成水和氧气,所以除去双氧水的方法是加热;
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;加热;
(6)①根据图象知,随着pH的增大,汞的吸收率先减小后增大;酸性条件下,高锰酸钾具有强氧化性,所以酸性条件下的高锰酸钾氧化性更强,
故答案为:随着pH的增大,汞的吸收率先减小后增大;高锰酸钾在酸性条件下氧化性强.
(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2 , 其负极上锌失电子发生氧化反应;
(2)高温下,氯化铵易分解;
(3)操分离不溶性固体和溶液采用过滤的方法;
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①根据二氧化锰和转移电子之间的关系式计算;
②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水;
(5)酸性条件下,双氧水能将铜氧化生成铜离子;加热条件下,双氧水易分解;
(6)根据横坐标与其吸收率曲线变化趋势分析;酸性条件下,高锰酸钾具有强氧化性.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.合成纤维和人造纤维统称为化学纤维
B.聚氯乙烯是热固性塑料
C.锦纶丝接近火焰时先蜷缩,燃烧时有烧焦羽毛的气味,灰烬为有光泽的硬块,能压成粉末
D.对于某些合成材料和塑料制品废弃物的处理可以倾倒到海洋中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图中氮元素及其化合物的转化关系,回答问题:
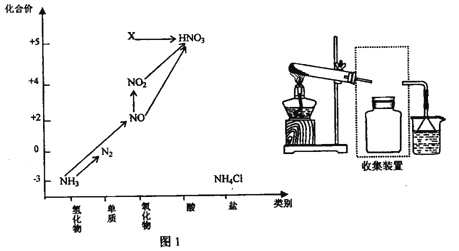
(1)实验窒常用NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为___________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。___________
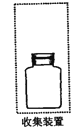
(3)下列试剂不能用手干燥NH3的是_________。
A.浓硫酸 B.碱石灰 C.NaOH 固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO 化学方程式为____________。
②NO→NO2 实验现象是_______ 。
③ NO2![]() HNO3 氧 化剂 与 还原剂物质的量之比为_______。
HNO3 氧 化剂 与 还原剂物质的量之比为_______。
(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,则该物质的化学式为_____________,
(6) 图1中,X的化学式为__________,从物质性质上看,X 属于_______氧化物。
(7)若要将NH3→N2,,从原理上看,下列试剂可行的是_______。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇单质碘→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
⑥用稀盐酸酸化Fe(NO3)2→变黄
⑦浓硝酸涂在蓝色石蕊试纸→变红
⑧Fe(OH)3胶体通电一段时间→正极附近颜色加深
A.①②③④⑥ B.②③④⑤⑦ C.①②④⑤⑥ D.①③④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.常温常压下,1mol丙烷共用电子对数为10 NA
B.0.5 mol甲烷和0.5 mol乙酸完全燃烧消耗的O2分子数都为0.2NA
C.标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为 ![]() NA
NA
D.1 mol甲醇与足量钠反应,转移电子数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按下列要求填空:
(1)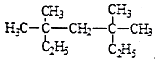 系统命名法为;
系统命名法为;
(2)键线式 ![]() 表示的有机物的结构简式是;
表示的有机物的结构简式是;
(3)醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是 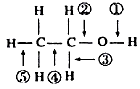
①和金属钠作用时,断裂;
②和浓硫酸共热至170℃时,断裂;
③和乙酸、浓硫酸共热时,断裂;
④在铜催化下和氧气反应时,断裂;
⑤与氢卤酸反应时,断裂;
(4)分子质量为70的烯烃的分子式为 , 若该烯烃与足量H2加成后能生成含3个甲基的烷烃,则该烯烃可能的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏伽德罗常数,则关于热化学方程式:C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(l)△H=﹣1300kJmol﹣1的说法中,正确的是( )
O2(g)═2CO2(g)+H2O(l)△H=﹣1300kJmol﹣1的说法中,正确的是( )
A.当有6 NA个电子转移时,该反应放出1300 kJ的能量
B.当有NA个水分子生成且为液体时,吸收1300 kJ的能量
C.当有4NA个碳氧共用电子对生成时,放出1300 kJ的能量
D.当有8NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面是4种粒子的结构示意图:
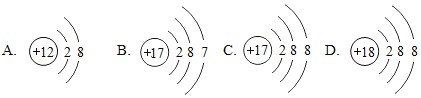
图中粒子共能表示_______种元素,图中表示的阳离子是____________(用离子符号表示),图中A所表示的元素在元素周期表中的位置_____________________________.
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
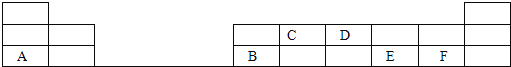
①写出D单质的电子式_____________________;
②写出C的最高价氧化物的结构式_____________________;
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________________;
④A最高价氧化物的水化物所含化学键为___________________,其晶体类型为________,其水溶液与B反应的离子方程式为___________________________;
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是 (______)
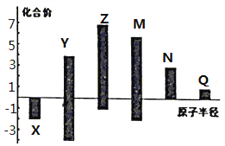
A.金属性:N>Q B.最高价氧化物对应水化物酸性:M>Y>N
C.简单离子半径:Q>N>X D.原子序数:Z>M>X>Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com