
A.CH2=CH2 B.SO
科目:高中化学 来源: 题型:





查看答案和解析>>
科目:高中化学 来源: 题型:


| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源:2012届山西省山大附中高三第一次模拟试题理综化学试卷(带解析) 题型:填空题
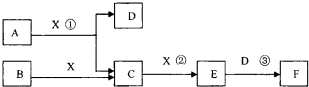
(14分)已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。(某些产物可能略去)
请回答下列问题:
(1)若E是有色气体,F是一元强酸,反应①是工业制备F的第一步反应。
①写出A与X反应的化学方程式: 。
②有人认为“浓H2SO4可以干燥气体E”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且浓H2SO4由无色变为红棕色,由此你得出的结论是 。
③已知常温下1 mol气体E发生反应③放出46kJ热量,写出气体E与H2O反应的热化学方式 。
④在常温下,向V1L pH=a的A溶液中加入V2L pH=b的盐酸,且a+b=14,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(填>、<、无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是 。(写出一种情况即可)
(2)若E为无色无味气体,F是二元弱酸。
①E的电子式为 ;
②将少量气体E通入氢氧化钡溶液中得不溶物G,G的KSP=8.1×10-9。现将该沉淀放入0.1mol/L的BaCl2溶液中,其KSP ,(填:增大、减小或不变),此时,组成不溶物G的阴离子在溶液中的浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省宁德市高三5月质检理综化学试卷(解析版) 题型:填空题
甲、乙、丙、丁、X是由短周期元素组成的纯净物,其中X为单质。上述物质转化关 系如下图所示(某些产物略去)。

请回答下列问题:
(1)若丁是一元强酸,甲→丁是工业生产丁的主要途径。
①写出反应I的化学方程式: 。
②常温下,1 mol丙发生反应III放出46kJ热量,该反应的热化学方程式为: 。
③在常温下,向V1L pH= 11的甲溶液中加入V2L pH=3的盐酸,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(选填“>”、“<”或“=”),所得溶液中各种离子的浓度由大到小的顺序可能是: (写一种即可)。
(2)若丁是二元弱酸,丙是温室气体。
在容积为2L的容积固定的密闭容器中,将乙(g)和H2O(g)按下表用量分别进行反应:乙(g)+H2O(g)  丙(g) + H2(g),得到如下数据:
丙(g) + H2(g),得到如下数据:

①该反应的正反应为 (填“吸热”或“放热”)反应。
②900℃时,上述反应按如下起始量分别加入该容器:

则此时反应的v(正) v(逆)(填“>”、“<”或“=”)。
③实验3跟实验2相比,改变的条件可能是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省高三第一次模拟试题理综化学试卷(解析版) 题型:推断题
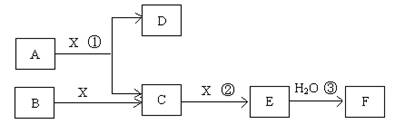
(14分)已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。(某些产物可能略去)
请回答下列问题:
(1)若E是有色气体,F是一元强酸,反应①是工业制备F的第一步反应。
①写出A与X反应的化学方程式: 。
②有人认为“浓H2SO4可以干燥气体E”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且浓H2SO4由无色变为红棕色,由此你得出的结论是 。
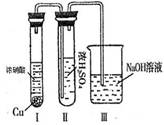
③已知常温下1 mol气体E发生反应③放出46kJ热量,写出气体E与H2O反应的热化学方式 。
④在常温下,向V1L pH=a的A溶液中加入V2L pH=b的盐酸,且a+b=14,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(填>、<、无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是 。(写出一种情况即可)
(2)若E为无色无味气体,F是二元弱酸。
①E的电子式为 ;
②将少量气体E通入氢氧化钡溶液中得不溶物G,G的KSP=8.1×10-9。现将该沉淀放入0.1mol/L的BaCl2溶液中,其KSP ,(填:增大、减小或不变),此时,组成不溶物G的阴离子在溶液中的浓度为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com