
【题目】由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用材料
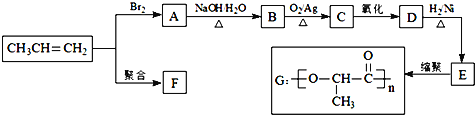
(1)E中官能团的名称_________.
(2)写出D的结构简式_________.
(3)聚合物F的结构简式是____________________.
(4)B转化为C的化学方程式是______________________________.
(5)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是_________.
(6)E有多种同分异构体,写出与E含有相同官能团的同分异构体的结构简式_________,其核磁共振氢谱显示为__________组峰,峰面积之比为______________。
【答案】 羧基、羟基 ![]()
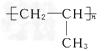
 +O2
+O2![]()
![]() +2H2O
+2H2O 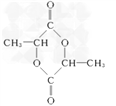 HOCH2CH2COOH 4 1:2:2:1
HOCH2CH2COOH 4 1:2:2:1
【解析】丙烯与溴发生加成反应生成A,A为CH3CHBrCH2Br,A在氢氧化钠水溶液加热条件下发生水解反应生成B,B为CH3CH(OH)CH2OH,B催化氧化生成C,C为![]() ,C氧化生成D,D为
,C氧化生成D,D为![]() ,D与氢气发生加成反应生成E,E为CH3CH(OH)COOH,E发生酯化反应是高聚物G,丙烯发生加聚反应生成高聚物F,F为
,D与氢气发生加成反应生成E,E为CH3CH(OH)COOH,E发生酯化反应是高聚物G,丙烯发生加聚反应生成高聚物F,F为![]() 。则(1)E为CH3CH(OH)COOH,官能团的名称为羧基、羟基;(2)D的结构简式为
。则(1)E为CH3CH(OH)COOH,官能团的名称为羧基、羟基;(2)D的结构简式为![]() ;(3)聚合物F的结构简式是
;(3)聚合物F的结构简式是![]() ;(4)B催化氧化生成C的化学方程式是(4). CH3CH(OH)CH2OH+O2
;(4)B催化氧化生成C的化学方程式是(4). CH3CH(OH)CH2OH+O2![]()
![]() +2H2O;(5)在一定条件下,两分子E[CH3CH(OH)COOH]能脱去两分子水形成一种六元环化合物,该化合物是环酯,其结构简式是
+2H2O;(5)在一定条件下,两分子E[CH3CH(OH)COOH]能脱去两分子水形成一种六元环化合物,该化合物是环酯,其结构简式是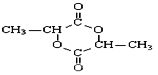 ;(6)E有多种同分异构体,与E含有相同官能团的同分异构体是位置异构,其结构简式为HOCH2CH2COOH,根据结构简式可知,其核磁共振氢谱显示为4组峰,峰面积之比为1:2:2:1。
;(6)E有多种同分异构体,与E含有相同官能团的同分异构体是位置异构,其结构简式为HOCH2CH2COOH,根据结构简式可知,其核磁共振氢谱显示为4组峰,峰面积之比为1:2:2:1。


科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法正确的是
物质 | 杂质 | 试剂 | 主要操作 | |
A | NaHCO3 | Na2CO3 | ---- | 灼烧 |
B | SiO2 | Fe2O3 | 盐酸 | 过滤 |
C | KBr溶液 | Br2 | KOH溶液 | 分液 |
D | Cl2 | HCl | 饱和碳酸钠溶液 | 洗气 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出H+和Clˉ
B.NaOH是离子化合物,该物质中只含有离子键
C.HI气体受热分解的过程中,只需克服分子间作用力
D.石英和干冰均由原子构成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:

⑴氯化水解法生产三氯氧磷的化学方程式为______。
⑵通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是______(选填字母),滴定终点的现象为______。
a.NH4Fe(SO4)2 b.FeCl2 c.甲基橙 d.淀粉
②实验过程中加入硝基苯的目的是_____________________,如无此操作所测Cl元素含量将会______(填“偏大”、“偏小”或“不变”)
⑶氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是_________________。
②下图是不同条件对磷的沉淀回收率的影响图像。
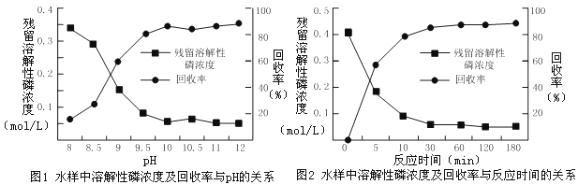
处理该厂废水最合适的工艺条件为______(选填字母)。
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7mol·L-1,溶液中c(Ca2+)=__________mol·L-1。
(已知Ksp[Ca3(PO4)2]=2×10-29)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是( )
选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
A | NH3(H2O) | 浓硫酸 | 洗气 |
B | KCl固体(I2) | KOH溶液 | 加热 |
C | H2O(Br2) | CCl4 | 分液 |
D | Cl2(HCl) | KOH溶液 | 洗气 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对盐类物质可有下列分类:如氯化硝酸钙[Ca(NO3)Cl]是一种混盐,硫酸铝钾KAl(SO4)2是一种复盐,冰晶石(六氟合铝酸钠)Na3AlF6是一种络盐。对于组成为CaOCl2的盐可归类于( )
A. 混盐 B. 复盐 C. 络盐 D. 无法归属于上述类别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图所示为锌铜原电池。下列叙述中,正确的是
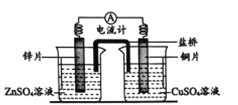
A. 盐桥的作用是传导离子
B. 外电路电子由铜片流向锌片
C. 锌片上的电极反应式为Zn2+ +2e- = Zn
D. 外电路中有0.2 mol 电子通过时,铜片表面增重约3.2 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com