
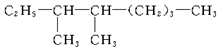 名称:2,3-二甲基辛烷
名称:2,3-二甲基辛烷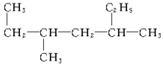 名称:3,5-二甲基庚烷.
名称:3,5-二甲基庚烷. 分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:(1)物质为烷烃,选取最长碳链为主碳链含8个,离取代基近的一端编号,写出名称为2,3-二甲基辛烷,故答案为:2,3-二甲基辛烷;
(2)物质为烷烃,选取最长碳链为主碳链含7个,离取代基近的一端编号,写出名称为3,5-二甲基庚烷,故答案为:3,5-二甲基庚烷.
点评 本题考查了有机物系统命名方法的应用,注意主链选择,起点编号原则,名称书写的规范方法,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 5 | C. | 4 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀硫酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 红热的焦炭与水蒸气的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4H+C→CH4 | B. | CuSO4•5H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+5H2O | ||
| C. | CaO+H2O=Ca(OH)2 | D. | CO2(g)→CO2(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
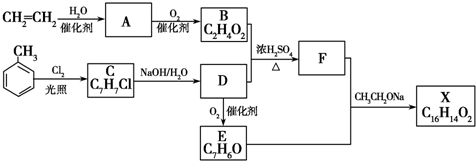
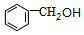 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O.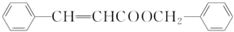 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.
A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.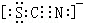 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,5.6g Fe与足量Cl2充分反应转移电子总数为0.2NA | |
| B. | 密闭容器中2molNO与1molO2充分反应后,容器内气体的分子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 1 L 0.lmol•L-1的CH3COONa溶液中CH3COO-和CH3COOH粒子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
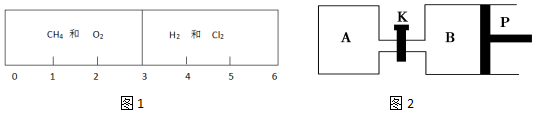
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| A | 78 | 0.8786 | 80 | A,B,C互溶 |
| B | 74 | 0.81018 | 108 | |
| C | 130 | 0.8670 | 142 |
| A. | 不能用蒸馏的方法进行分离 | |
| B. | 可以用过滤的方法进行分离 | |
| C. | 若采用蒸馏操作,冷凝管中冷却水的流向应该与蒸气的流向相反 | |
| D. | 该实验中用到的玻璃仪器有:酒精灯、蒸溜烧瓶、冷凝管、接液管、锥形瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com