
【题目】下列物质不属于合金材料的是( )
A.赤铁矿B.硬铝C.304不锈钢D.青铜器
科目:高中化学 来源: 题型:
【题目】六种短周期元素在元素周期表中的相对位置如图所示,其中R元素的最外层电子数是其次外层电子数的一半。

请回答下列问题:
(1)R的元素名称是_______,中子数为8的X元素的原子是______(用原子组成符号表示)。
(2)上述六种元素,非金属性最强的元素为________________(填元素符号)
(3)Z的最高价氧化物对应水化物的化学式为____________________。
(4)W和Y形成一种二元化合物甲的相对分子质量为184,且Y的质量分数约为30%。则化合物甲的化学式为__________________。化合物甲在摩擦时会发生猛烈爆炸,分解为一种W的单质和一种Y的单质,其中W的单质与Y的单质的相对分子质量之比为64∶7。写出化合物甲爆炸分解的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】称取铁粉和氧化铜的混合物6.40g,进行如下实验: 
根据实验所得数据,下列说法不正确的是( )
A.原混合物中铜元素的质量一定为0.64g
B.生成气体体积为2.016L
C.实验中反应的硫酸的物质的量为0.1mol
D.原混合物中铁的质量分数为87.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石和碱式碳酸铝镁[MgaAlb(OH)c(CO3)dxH2O]在生产生活中都有着极为重要的应用.某研究小组对用明矾石制取氢氧化铝等物质,以及碱式碳酸铝镁的组成展开了如下研究,请你参与并完成对有关问题的解答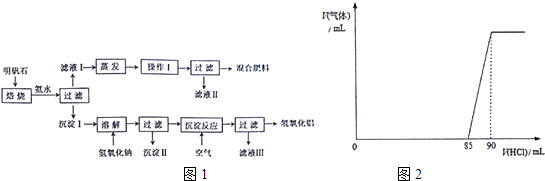
(1)明矾石是制取化肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质.具体实验步骤如图1所示:①操作I的名称为
②混合肥料的主要成分是(写化学式).检验滤液Ⅱ中是否含有NH4+的方法是:取少货滤液Ⅱ于试管中,向其中加入适量的NaOH溶液,加热,若产生气体能够使 , 则证明滤液Ⅱ中含有NH4+
③一定条件下,下列物质能与沉淀Ⅱ发生反应的是(填字母)
a.KSCN溶液 b.Al c.NaOH 溶液
④空气能够为沉淀反应提供足量的(写化学式).
(2)碱式碳酸铝镁是常见胃药“达喜”的主要成分.为确定碱式碳酸铝镁的组成,进行了如下实验:①取碱式碳酸铝镁粉末6.02g,缓缓加入2.0molL﹣1盐酸使其充分混合反应,反应过程中产生气体的体积V(气体)和消耗盐酸的体积V(HC1)的关系如图2所示,则碱式碳酸铝镁中氢氧根与碳酸根的物质的量之比为
②将①反应后得到的混合液再和过量的氢氧化钠溶液充分混合,反应完全后经过过滤、洗涤、干燥得沉淀3.48g,则碱式碳酸铝镁的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是石蜡油在炽热碎瓷片的作用下产生某气体并检验其性质的相关实验,请完成下列问题:
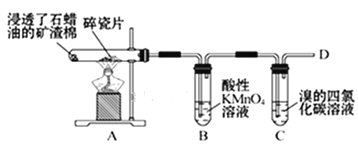
(1)A中产生的气体是___________(填名称),该物质的结构式__________________________;
(2)B中实验现象:_____________________,原因是:__________________________________;
(3)C中发生反应的化学方程式:_________________________________,反应类型:______________ ;
(4)在D处点燃时必须进行的操作_________________________________;
(5)下列说法正确的是(_______)
A.聚乙烯塑料可以用做食品袋、餐具和地膜
B.乙烯分子中所有原子不共面
C.高锰酸钾溶液浸泡过的硅藻土可以保鲜水果
D.乙烯是一种植物生产调节剂,可以延长果实和花朵的成熟期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是( )
A. 向水中通入SO2 B. 将水加热煮沸
C. 向纯水中投入一小块金属钠 D. 向水中加入NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸钾。现从草木灰中提取钾盐,并用实验检验其中的CO![]() 、SO
、SO![]() 和Cl-。
和Cl-。
(1)从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③________,④蒸发,⑤冷却结晶。
(2)在进行③、④操作时,都要用到玻璃棒,其作用分别是:③________;④________。
(3)将制得的少量晶体放入试管,加蒸馏水溶解并把溶液分成三份,分装在3支试管里。
①在第一支试管里加入稀盐酸,可观察有________生成,证明溶液中有________离子。
②在第二支试管里加入足量稀盐酸后,再加入BaCl2溶液,可观察到有________生成,证明溶液中有________离子。
③在第三支试管里加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量稀硝酸后,再加入AgNO3溶液,可观察到有________生成,证明溶液中有________离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有CO和CO2的混合气体20克,其在标准状况下的体积为11.2L。据此回答下列问题:
(1)该混合气体总的物质的量为______,其平均摩尔质量为_______。
(2)混合气体中碳原子的个数为________。(用NA表示阿伏加德罗常数的值)
(3)若将该混合气体全部通过下图装置进行实验。

则:①气球中收集的气体是______,其质量为_______ 克
②从A瓶中获得沉淀质量的操作是_____、称量。
③若要证明A瓶溶液中的阳离子是否沉淀完全,其方法为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com