
分析 (1)纤维素水解得到的最终产物A为葡萄糖,NaClO3生成ClO2,氯元素从+5价降到+4价,葡萄糖中碳从0价升到+4价,根据元素守恒和电荷守恒配平方程式;
(2)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,用钡离子除去硫酸根离子,用氢氧根除去镁离子,用碳酸根除去钙离子,同时注意除杂是示能引入新的杂质,据此判断加入试剂的顺序;
②根据氧化还原反应化合价升降规律,NaClO3与盐酸反应生成ClO2的同时会生成氯气,据此写出化学方程式;
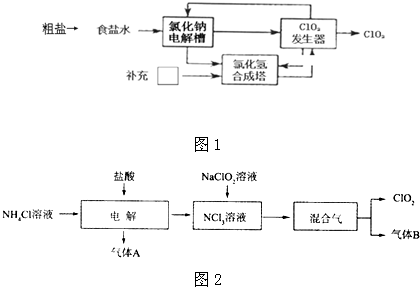
③根据图1流程可知,电解氯化钠溶液生成NaClO3的同时有氢气产生,被充适量的氯气后,氢气和氯气合成氯化氢,氯化氢再与NaClO3反应得ClO2,所以氯化钠和氯气都是流程中的原料,据此判断可循环利用的物质,电解槽阴极产生的气体应为氢气,方框中物质应为氯气,根据元素守恒可确定它们的物质的量之比;
(3)A气体在标准状况下的密度为0.089g/L,则A气体为氢气,(Ⅱ)气体B能使湿润的红色石蕊试纸变蓝,则B为氨气,
①根据流程可知,电解时反应物为氯化铵和盐酸,生成物为氢气和NCl3,据此书写化学方程式;
②NCl3与NaClO2按物质的量之比为1:6混合,在溶液中恰好反应生成ClO2,根据电荷守恒和元素守恒书写离子方程式;
解答 解:(1)纤维素水解得到的最终产物A为葡萄糖,NaClO3生成ClO2,氯元素从+5价降到+4价,葡萄糖中碳从0价升到+4价,反应的化学方程式为1 C6H12O6+24 NaClO3+12H2SO4=24 ClO2↑+6 CO2↑+18H2O+12 Na2SO4,
故答案为:1 C6H12O6+24 NaClO3+12H2SO4=24 ClO2↑+6 CO2↑+18H2O+12 Na2SO4;
(2)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,用钡离子除去硫酸根离子,用氢氧根除去镁离子,用碳酸根除去钙离子,同时注意除杂是示能引入新的杂质,碳酸根离子要放在最后加入,所以加入试剂的顺序为BaCl2、NaOH和Na2CO3或NaOH、BaCl2和Na2CO3,
故答案为:BaCl2、NaOH和Na2CO3或NaOH、BaCl2和Na2CO3;
②根据氧化还原反应化合价升降规律,NaClO3与盐酸反应生成ClO2的同时会生成氯气,反应的化学方程式为2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O,
故答案为:2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O;
③根据图1流程可知,电解氯化钠溶液生成NaClO3的同时有氢气产生,被充适量的氯气后,氢气和氯气合成氯化氢,氯化氢再与NaClO3反应得ClO2,所以氯化钠和氯气都是流程中的原料,结合电解槽和ClO2发生器中产物可知,可循环利用的物质是NaCl、Cl2,电解槽阴极产生的气体应为氢气,方框中物质应为氯气,根据根据反应NaCl+3H2O$\frac{\underline{\;电解\;}}{\;}$NaClO3+3H2及反应2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O,可知反应中产生的H2、Cl2的物质的量之比为6:1,而反应中H2、Cl2的物质的量之比为1:1,要使原子的利用率为100%,则产生的H2和要补充的氯气的物质的量之比为6:5,
故答案为:NaCl、Cl2;6:5;
(3)A气体在标准状况下的密度为0.089g/L,则A气体为氢气,(Ⅱ)气体B能使湿润的红色石蕊试纸变蓝,则B为氨气,
①根据流程可知,电解时反应物为氯化铵和盐酸,生成物为氢气和NCl3,所以化学方程式为NH4Cl+2HCl$\frac{\underline{\;电解\;}}{\;}$3H2↑+NCl3,
故答案为:NH4Cl+2HCl$\frac{\underline{\;电解\;}}{\;}$3H2↑+NCl3;
②NCl3与NaClO2按物质的量之比为1:6混合,在溶液中恰好反应生成ClO2,根据电荷守恒和元素守恒可知其离子方程式为NCl3+6ClO2-+3H2O=6ClO2↑+NH3↑+3Cl-+3OH-,
故答案为:NCl3+6ClO2-+3H2O=6ClO2↑+NH3↑+3Cl-+3OH-.
点评 本题考查氧化还原反应、常用化学用语、电解原理、化学计算等,题目难度中等,电解反应是难点、易错点,是对学生综合能力的考查,需要学生具有扎实的基础与分析解决问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、SiO2、P2O5均为酸性氧化物 | |
| B. | 是否具有丁达尔效应是胶体与溶液、浊液的根本区别 | |
| C. | 纯净盐酸为纯净物、冰水混合物为混合物 | |
| D. | 烧碱、纯碱都属于碱,油脂、甘油都属于酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取10.6gNaCO3,加入100mL容量瓶中,加水溶解,定容 | |
| B. | 称取10.6gNaCO3,加入100mL蒸馏水,搅拌,溶解 | |
| C. | 移液时未用玻璃棒引流,直接倒入容量瓶中 | |
| D. | 定容后,反复倒转,摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2C2H5OH
+2C2H5OH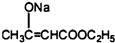 +CH3COOH→
+CH3COOH→ +CH3COONa
+CH3COONa
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 1.9 | 7.0 | 3.4 |
| 完全沉淀的pH | 3.2 | 9.0 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学以甘蔗渣为原料用水解一氧化一水解循环进行制取草酸并探究测定草酸晶体(H2C2O4•xH2O)的某些性质.通过查阅资料可知:草酸易溶于水,是一种重要的化工原料,广泛用于药物生产、高分子合成等工业,草酸晶体受热到100℃时失去结晶水,成为无水草酸.157℃时大量升华,并开始分解;草酸蒸气在低温下可冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊.
某同学以甘蔗渣为原料用水解一氧化一水解循环进行制取草酸并探究测定草酸晶体(H2C2O4•xH2O)的某些性质.通过查阅资料可知:草酸易溶于水,是一种重要的化工原料,广泛用于药物生产、高分子合成等工业,草酸晶体受热到100℃时失去结晶水,成为无水草酸.157℃时大量升华,并开始分解;草酸蒸气在低温下可冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊.

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=C(CH3) CH3 3-甲基-2-丁烯 | |
| B. | CH3CH(CH3)CH(Cl)CH3 3-甲基-2-氯丁烷 | |
| C. | CH3CH(OH)CH2CH3 2-羟基丁醇 | |
| D. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com