
 ;
;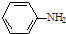 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸( 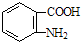 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)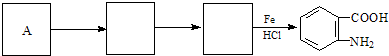
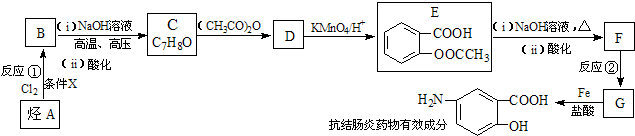
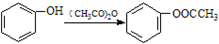
分析 C发生信息(a)中的反应生成D,D发生氧化反应生成E,结合C的分子式与E的结构简式,可知C的结构简式为 ,则D为
,则D为 ,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为 ,B为
,B为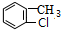 ;E与氢氧化钠反应、酸化得到F为
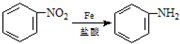
;E与氢氧化钠反应、酸化得到F为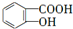 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为 ,G发生还原反应得到抗结肠炎药物有效成分;
,G发生还原反应得到抗结肠炎药物有效成分;
(4)甲苯和浓硝酸发生取代反应生成邻甲基硝基苯,邻甲基硝基苯和酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸和Fe、HCl反应生成邻氨基苯甲酸,据此分析解答.
解答 解:C发生信息(a)中的反应生成D,D发生氧化反应生成E,结合C的分子式与E的结构简式,可知C的结构简式为 ,则D为
,则D为 ,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为 ,B为
,B为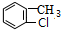 ;E与氢氧化钠反应、酸化得到F为
;E与氢氧化钠反应、酸化得到F为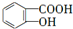 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为 ,G发生还原反应得到抗结肠炎药物有效成分,
,G发生还原反应得到抗结肠炎药物有效成分,
(1)根据其结构简式确定分子式为C7H7O3N,反应①是苯环上发生的取代反应,该反应的反应条件是Fe或FeCl3 作催化剂,反应②为取代反应,
故答案为:C7H7O3N;Fe或FeCl3;取代反应;
(2)①A.该物质中含有亲水基酚羟基、羧基和氨基,所以水溶性比苯酚好,故正确;
B.含有氨基和羧基,所以能发生聚合反应,不能发生消去反应,故错误;
C.苯环上连接酚羟基邻位氢原子能和溴发生取代反应,所以1mol该物质最多可与1mol溴发生反应,故错误;
D.酚羟基和羧基具有酸性、氨基具有碱性,所以该物质既有酸性又有碱性,故正确;
故选A D;
②E中酯基和羧基都与NaOH反应,该反应方程式为: ,
,
故答案为: ;
;
(3)其同分异构体符合下列条件:
a.遇FeCl3溶液有显色反应,说明含有酚羟基;
b.分子中甲基与苯环直接相连;
c.苯环上共有三个取代基,三个取代基分别是硝基、甲基和酚羟基,
如果硝基和甲基处于邻位,有4种结构;
如果硝基和甲基处于间位,有4种结构;
如果硝基和甲基处于对位,有2种结构,所以符合条件的有10种同分异构体,
故答案为:10;
(4)甲苯和浓硝酸发生取代反应生成邻甲基硝基苯,邻甲基硝基苯和酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸和Fe、HCl反应生成邻氨基苯甲酸,其合成路线为 ,两种中间产物的结构简式为
,两种中间产物的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物推断和有机合成,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查学生分析判断及知识综合运用能力,难点是合成路线设计和同分异构体种类判断,注意题给信息的正确筛取和运用,题目难度中等.


科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下能实现的是
A.Fe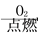 Fe2O3
Fe2O3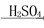 Fe2(SO4)3
Fe2(SO4)3
B.MgO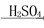 MgSO4(aq)
MgSO4(aq)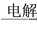 Mg
Mg
C.饱和NaCl(aq)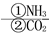 NaHCO3
NaHCO3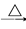 Na2CO3
Na2CO3
D.NH3 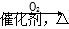 NO
NO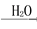 HNO3
HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
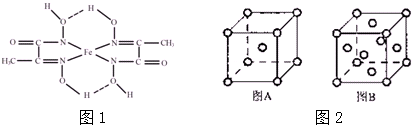
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能使酸性高锰酸钾溶液褪色 | |
| B. | 乙烯可以燃烧 | |
| C. | 苯能使酸性高锰酸钾溶液褪色 | |
| D. | 苯通常易发生取代反应较难发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
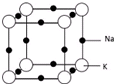 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.
2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
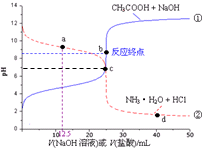
| A. | a点:c(Cl-)>c(NH3•H2O)>c(NH4+) | B. | b点:c(OH-)=c(H+)+c(CH3COOH) | ||
| C. | c点:c(NH4+)=c(CH3COO-) | D. | d点:c(NH4+)>c(Cl-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,1mol氦气含有的原子数为NA | |
| B. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| C. | 常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 | |
| D. | 物质的量浓度为1 mol•L-1的K2SO4溶液中,含2NA个K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com