



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ČēÓŅæņĶ¼·“Ó¦ÖŠĖłÉę¼°µÄl4ÖÖĪļÖŹ¶¼ŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄ£®ŅŃÖŖ£ŗ
ČēÓŅæņĶ¼·“Ó¦ÖŠĖłÉę¼°µÄl4ÖÖĪļÖŹ¶¼ŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄ£®ŅŃÖŖ£ŗ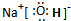
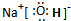
| ||
| ”÷ |
| ||
| ”÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| ||
| ||

t£Ømin£© ÅØ¶Č£Ømol/L£© |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c£ØC£© | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c£ØO2£© | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēÓŅæņĶ¼·“Ó¦ÖŠĖłÉę¼°µÄl4ÖÖĪļÖŹ¶¼ŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄ£®ŅŃÖŖ£ŗ
ČēÓŅæņĶ¼·“Ó¦ÖŠĖłÉę¼°µÄl4ÖÖĪļÖŹ¶¼ŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄ£®ŅŃÖŖ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

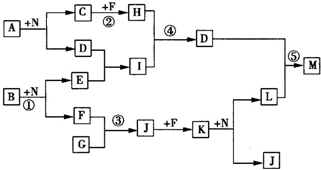
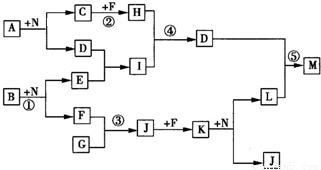
ŅŃÖŖ£ŗ£Ø1£©¼×ŗĶŅŅµÄ×é³ÉŌŖĖŲĻąĶ¬£¬¾łŹĒÓÉĮ½ÖÖ³£¼ūŌŖĖŲµÄŌ×ÓŅŌ×ī¼ņÕūŹż±Č¹¹³ÉµÄ»ÆŗĻĪļ£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæ·Ö±šĪŖ124”¢180”££Ø2£©C”¢D”¢H”¢I”¢J³£ĪĀĻĀĪŖĘųĢ壬H”¢I”¢JĪŖµ„ÖŹ£¬DŹĒŅ»ÖÖŗģ×ŲÉ«ĘųĢ壬NĪŖŗģŗÖÉ«¹ĢĢ唣£Ø3£©·“Ó¦¢ŚĪŖÖʱøĄķĻėµÄĀĢÉ«Ė®“¦Ąķ¼ĮNa2FeO4£ØøßĢśĖįÄĘ£©µÄŅ»ÖÖ·½·Ø”££ØĶ¼ÖŠ²æ·ÖÉś³ÉĪļƻӊĮŠ³ö£©
ĒėĢīŠ“ŅŌĻĀæÕ°×£ŗ
£Ø1£©Š“³öCµÄµē×ÓŹ½______________”£
£Ø2£©Š“³ö·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½______________”£
·“Ó¦¢ŚµÄĄė×Ó·½³ĢŹ½_________________”£
£Ø3£©¼×ŗĶŅŅµÄ»ÆѧŹ½·Ö±šĪŖ________”¢________£¬
ČōAÖŠ×é³ÉŌŖĖŲµÄĪļÖŹµÄĮæÖ®±ČĪŖ4”Ć9£¬ŌņŅŅŌŚAÖŠµÄĪļÖŹµÄĮæ·ÖŹżĪŖ________________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013Äźøßæ¼»Æѧ±øæ¼ø“Ļ°¾ķC12£ŗ³£¼ūŌŖĖŲ¼°ĘäÓ¦ÓĆ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com