
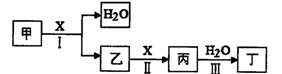
 ��(g) + H2(g)���õ��������ݣ�
��(g) + H2(g)���õ��������ݣ�

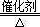 4NO+6H2O��3�֣�
4NO+6H2O��3�֣�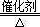 4NO+6H2O�����������֪��NO2(g)+1/3H2O(l)=2/3HNO3(aq)+1/3NO(g) ��H=��46kJ/mol����3NO2(g)+H2O(l)==2HNO3(aq)+NO(g) ��H=��138kJmol��1������V1=V2����c(NH3?H2O)>c(HCl)����c?V��֪�������������Һ�ʼ��ԣ���V1<V2�������Һ�ſ��������ԣ�����������̶Ƚ�С�������Ի����Һ��c(Cl��)>c(NH4+)>c(H+)>c(OH��)������������̶Ƚϴ���c(Cl��)>c(H+)>c(NH4+)>c(OH��)����2��������֪��Ϣ��֪���ס��ҡ���������X�ֱ���C��CH4��CO��CO2��H2CO3��O2����
4NO+6H2O�����������֪��NO2(g)+1/3H2O(l)=2/3HNO3(aq)+1/3NO(g) ��H=��46kJ/mol����3NO2(g)+H2O(l)==2HNO3(aq)+NO(g) ��H=��138kJmol��1������V1=V2����c(NH3?H2O)>c(HCl)����c?V��֪�������������Һ�ʼ��ԣ���V1<V2�������Һ�ſ��������ԣ�����������̶Ƚ�С�������Ի����Һ��c(Cl��)>c(NH4+)>c(H+)>c(OH��)������������̶Ƚϴ���c(Cl��)>c(H+)>c(NH4+)>c(OH��)����2��������֪��Ϣ��֪���ס��ҡ���������X�ֱ���C��CH4��CO��CO2��H2CO3��O2���� CO2(g) + H2(g)
CO2(g) + H2(g)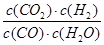 =
=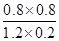 =8/3
=8/3 CO2(g) + H2(g)
CO2(g) + H2(g)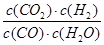 =
=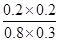 =1/6
=1/6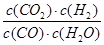 =
=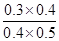 =3/5>1/6��˵���÷�ӦӦ���淴Ӧ�����ƶ������ܴﵽ���¶��µĻ�ѧƽ�⣬��v(��)>v(��)��ʵ��2��3��ƽ��û���ƶ�������Ӧ���ʼӿ죬˵��2��3����ʹ���˴�����
=3/5>1/6��˵���÷�ӦӦ���淴Ӧ�����ƶ������ܴﵽ���¶��µĻ�ѧƽ�⣬��v(��)>v(��)��ʵ��2��3��ƽ��û���ƶ�������Ӧ���ʼӿ죬˵��2��3����ʹ���˴�����

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������X����NaOH��Һ��Ӧ�ų�H2��������Y���ܣ���Y�Ľ�����һ����X�� |
| B���ںϳɰ���Ӧ�ﵽƽ��ʱ��ֻ����N2�����ʵ���������ƽ���N2�İٷֺ������� |
| C���������϶�ͭʱ�����͵�Դ����������ͭ�������������������Һ��CuSO4��Һ |
| D��Cl2��SO2�������ֻ�Ϻ�ͨ��Ʒ����Һ����Һ��ɫû�����Ա仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2��SO3��H2SO4 | B��Al2O3��Al(OH)3��NaAlO2 |
| C��FeCl2��Fe(OH)2��Fe(OH)3 | D��NO��NO2��HNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
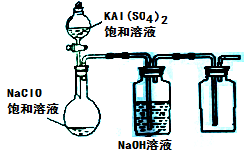
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ʵ����������� | ʵ��Ŀ�Ļ���� |
| A | �ýྻ��˿պȡ��Һ������ɫ��Ӧ������ʻ�ɫ | ԭ��Һ����Na+��K+ |
| B | ��0.1 mol/L��NaHCO3��Һ�У���2�η�̪��dz��ɫ���ȣ���Һ��ɫ���� | ��֤����ˮ�ⷴӦ�����ȷ�Ӧ |
| C | �����Ӵ�ú����ȡ�������ƣ������̶���С���ƿ飬����ֽ�����ƿ�����ú�ͣ�С�ķ���װ�б���ˮ���Թ��У��ƿ��ڱ���ˮ�������¸��� | �Ƚ��ơ�ˮ�ͱ��������ʵ��ܶȴ�С |
| D | ��Na2CO3��Һ��ͨ������CO2����Һ����� | NaHCO3���ܽ�ȱ�Na2CO3��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������Cl2����ˮ����ʹ�ʻ���ɫ |
| B�����ˮ��ͨ��SO2����ˮ��ɫ˵��SO2����Ư���� |
| C����FeBr2��Һ�еμ�������ˮ����Һ��dz��ɫ����Ϊ������Br2 |
| D����Cl2ͨ��AgNO3��Һ�в����г������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2��H218O��Ӧʱ����18O2���� |
B����2SO2��g��+O2��g�� 2SO3��g����ƽ����ϵ�м���18O2�����18Oֻ������SO3�� 2SO3��g����ƽ����ϵ�м���18O2�����18Oֻ������SO3�� |
| C��CH3COOH��CH3CH218OH����������Ӧʱ������ˮ�ķ���ʽΪH218O |
| D���ö��Ե缫��⺬��H218O��ˮʱ�����������������Է���������ͬ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������ˮ��Һ�ڳ����µ�PH<7�����һ��ΪHCl |
| B�����ҵ�Ħ��������O2��ͬ������һ��ΪN2H4 |
| C����3.0g�ı������ʵ���Ϊ0.lmol�����һ��Ϊ�����ͬϵ�� |
| D������Ϊ��ԭ�ӷ��ӣ���һ����ʹƷ����Һ��ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com