
| A. | 将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 | |
| B. | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | |
| C. | 向50mL12mol•L-1的浓硝酸中加入足量铜片其充分反应,生成0.3molNO2 | |
| D. | 运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
分析 浓硫酸具有强氧化性,可与金属锌、铜等反应生成二氧化硫气体,但稀硫酸与铜不反应,稀硫酸与活泼金属反应生成氢气,以此解答.
解答 解:A.浓硫酸和锌反应生成SO2,随着反应的进行,硫酸浓度逐渐降低,稀硫酸与锌反应生成氢气,故A错误;
B.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,酸性条件下,NO3-与Fe2+发生氧化还原反应生成NO,NO在试管口被氧化生成红棕色的二氧化氮气体,故B正确;
C.由于Cu足量,则浓硝酸完全反应,被还原的硝酸生成NO2、NO,由N元素守恒可知:2n[Cu(NO3)2]+n(气体)=n(HNO3)=0.05L×12mol/L=0.6mol,生成气体只有NO2时,被还原的硝酸达极大值,根据电子转移守恒2n[Cu(NO3)2]=n(NO2),联立方程解得:n(NO2)=0.3mol,而随反应的进行浓硫酸要变稀硫酸,所以生成NO2小于0.3mol,故C错误;
D.运输保存浓硫酸的槽罐车一旦泄露后,如果用水冲洗,硫酸被稀释而生成氢气,易爆炸,故D错误;
故选B.
点评 本题考查浓硫酸的性质,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握浓硫酸、稀硫酸的性质的异同,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,0.4g D2气体分子含有的中子数小于0.2NA | |
| B. | 含有0.32g氧元素的二氧化硅中含有的硅氧键数目为0.02NA | |
| C. | 11.2L Cl2通入足量氢氧化钠溶液中充分反应,转移的电子数等于0.5NA | |
| D. | 7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.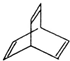 X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种.
X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种. .Y能使溴水褪色,其反应的化学方程式为
.Y能使溴水褪色,其反应的化学方程式为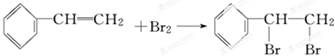 .Y可以用来合成一种聚合物---泡沫塑料,请写出该聚合物的结构简式
.Y可以用来合成一种聚合物---泡沫塑料,请写出该聚合物的结构简式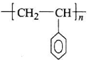 .有机化学中有多种同分异构现象,其中有顺反异构,请写出Y的侧链多一个甲基的有机物W的两种顺反异构的结构简式:
.有机化学中有多种同分异构现象,其中有顺反异构,请写出Y的侧链多一个甲基的有机物W的两种顺反异构的结构简式: ,
,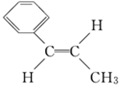 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和苯都能发生取代反应 | |
| B. | 乙醇和乙酸都能与氢氧化钠发生中和反应 | |
| C. | 乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 | |
| D. | 淀粉、油脂、蛋白质都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4:3:2 | B. | 1:2:1 | C. | 2:1:1 | D. | 1:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com