
��֪A��B��C��D��E��F���ֶ�����Ԫ�ص����ʻ�ṹ��Ϣ���±����������Ϣ�ش��������⡣
Ԫ�� ���ʻ�ṹ��Ϣ
A ���ʳ�����Ϊ���壬������ˮ������CS2�����γ�2�ֶ�Ԫ�����ᡣ
B ԭ�ӵ�M����1��δ�ɶԵ�p���ӡ�����p������������7��
C ����������Ϊ����ɫ�Ľ��ӡ�������γɵĺϽ����ں������������������ǿ���ǿ�
D ԭ�Ӻ�����Ӳ���s����������p����������2�������ʺ��������Ϊ�ռ���״���壬���кܸߵ��ۡ��е㡣
E ��������������β������Ҫ�к��ɷ�֮һ��Ҳ�ǿ�������Ԥ����ָ��֮һ����Ԫ���������谷�к����ϸߡ�
F ���ڱ��е縺������Ԫ��
��1��Aԭ�ӵ����������Ų�ʽ ��Dԭ�ӹ��� �ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2��F��EԪ�ص�һ�����ܵĴ�С��ϵ�� �� ����Ԫ�ط��ţ���
��3��A��B��Ԫ�ص��⻯������м��ܽ�С���� �����ӽ��ȶ����� ���������ʽ��
��4��C���ʡ�þ��NaOH��Һ���Թ���ԭ��أ����ĵ缫��ӦʽΪ_________________��
��5��F��ƿ�������ӻ�����侧���ṹ��ͼ��ʾ���û�����ĵ���ʽ�� ����֪�û����ᄃ��1/8�����Ϊ2.0��10-23cm3��������ӻ�������ܶȣ�����ʽ�����㣨�������һλС������_______________________��

��1��3s23p4��2�֣���14��1�֣�����2��N��F ����1�֣���2�֣�
 ��3��H2S��2�֣���HCl��2�֣� ��4��Al-3e-+4OH-
��AlO2-+2H2O��2�֣�
��3��H2S��2�֣���HCl��2�֣� ��4��Al-3e-+4OH-
��AlO2-+2H2O��2�֣�
��5��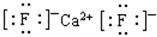 ��2�֣�
��2�֣�
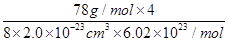 ��3.2 g/cm3����ʽ2�֣����1�֣���λ��1�֣�
��3.2 g/cm3����ʽ2�֣����1�֣���λ��1�֣�
��������
���������A�����ʳ�����Ϊ���壬������ˮ������CS2�����γ�2�ֶ�Ԫ�����ᣬ���A��S��B��ԭ�ӵ�M����1��δ�ɶԵ�p���ӣ�����p������������7����BӦ����Cl��C������������Ϊ����ɫ�Ľ��ӡ�������γɵĺϽ����ں������������������ǿ���ǿ�����C��Al��D��ԭ�Ӻ�����Ӳ���s����������p����������2�������ʺ��������Ϊ�ռ���״���壬���кܸߵ��ۡ��е㣬��D��Si��E����������������β������Ҫ�к��ɷ�֮һ��Ҳ�ǿ�������Ԥ����ָ��֮һ����Ԫ���������谷�к����ϸߣ���E��N��F�����ڱ��е縺������Ԫ����F����F�Ƿ�Ԫ�ء�
��1��SԪ��λ�ڵ������ڵڢ�A�壬����Sԭ�ӵ����������Ų�ʽΪ3s23p4��SiԪ�ص�ԭ��������14�������������14��������Siԭ�ӹ���14�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2���ǽ�����Խǿ����һ������Խ�����ڵ�Ԫ�ص�2p������Ӵ��ڰ����״̬���ȶ���ǿ�����һ�����ܴ��ڷ�Ԫ�صģ�����F��EԪ�ص�һ�����ܵĴ�С��ϵ��N��F��
��3���ǽ�������S����Cl����������Ԫ�ص��⻯������м��ܽ�С����H2S���ǽ�����Խǿ���⻯����ȶ���Խǿ����˷��ӽ��ȶ�����HCl��
��4��ԭ����нϻ��õĽ�����������þ�Ľ�����ǿ��Al�����������ܺ�����������Һ����þ���ܣ����Ե�������þ��NaOH��Һ���ɵ�ԭ��������Ǹ�����þ����������˸����ĵ缫��ӦʽΪAl-3e-+4OH- ��AlO2-+2H2O��
��5�����ݾ����Ľṹͼ�����ݾ�̯ԭ����֪����ԭ�ӵĸ�����8������ԭ�ӵĸ�����8�� ��6��
��6��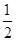 ��4������˸û�����Ļ�ѧʽΪCaF2���������Ӽ������ӻ������������ʽΪ
��4������˸û�����Ļ�ѧʽΪCaF2���������Ӽ������ӻ������������ʽΪ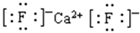 ����֪�û����ᄃ��1/8�����Ϊ2.0��10-23cm3����þ����������8��2.0��10-23cm3����˸��ݾ����и����ӵĸ�����4����֪
����֪�û����ᄃ��1/8�����Ϊ2.0��10-23cm3����þ����������8��2.0��10-23cm3����˸��ݾ����и����ӵĸ�����4����֪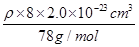 ��6.02��1023/mol��4����æѣ�
��6.02��1023/mol��4����æѣ�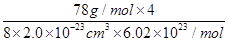 ��3.2 g/cm3��
��3.2 g/cm3��
���㣺����Ԫ���ƶϡ���������Ų�����һ�����ܱȽϡ����ܡ��⻯���ȶ����ж��Լ�����ṹ�뾧���ܶȵļ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ�
��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͨ������£���A��BΪ���ӣ�C��EΪ�����ӣ�DΪ�����ӣ����Ƕ�����10�����ӣ�B����A�����õ����ʿɵ����C��D��A��B��E��������Ӧ��ɵ�C��һ�ְ�ɫ��������ش�
����ͨ������£���A��BΪ���ӣ�C��EΪ�����ӣ�DΪ�����ӣ����Ƕ�����10�����ӣ�B����A�����õ����ʿɵ����C��D��A��B��E��������Ӧ��ɵ�C��һ�ְ�ɫ��������ش�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
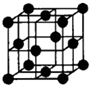
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe��Cu��Al��Ag | B��Al��Cu��Fe��Ag | C��Cu��Ag��Al��Fe | D��Ag��Al��Cu��Fe |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com