
| A. | 棉织物在灼烧时会产生烧焦羽毛的气味 | |
| B. | 氨基酸、淀粉、蛋白质均属于高分子化合物 | |
| C. | 将碘酒滴在土豆片上,可观察到土豆片变蓝色 | |
| D. | 利用油脂在酸性条件下的水解反应可以制取肥皂 |
分析 A.棉织物的成分为纤维素;
B.氨基酸的相对分子质量在10000以下;
C.土豆片含淀粉,淀粉遇碘变蓝;
D.油脂在碱性条件下水解为皂化反应.
解答 解:A.棉织物的成分为纤维素,而蛋白质在在灼烧时会产生烧焦羽毛的气味,故A错误;
B.氨基酸的相对分子质量在10000以下,不是高分子,而淀粉、蛋白质均属于高分子化合物,故B错误;
C.土豆片含淀粉,淀粉遇碘变蓝,则将碘酒滴在土豆片上,可观察到土豆片变蓝色,故C正确;
D.油脂在碱性条件下水解为皂化反应,酸性条件下不能得到肥皂,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的组成、性质、有机反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2、I2、HI的浓度相等 | B. | 混合气体的颜色不再改变 | ||
| C. | H2、I2、HI的浓度之比为1:1:2 | D. | 混合气体的平均相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第IA族的所有元素都是金属元素 | |
| B. | 同周期主族元素中,第ⅦA族元素原子半径最小 | |
| C. | 短周期元素形成离子后,最外层都达到8电子稳定结构 | |
| D. | -般在元素周期表的金属与非金属分界线附近寻找一些化学反应新型催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
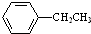 $→_{△}^{Fe_{2}O_{3}}$
$→_{△}^{Fe_{2}O_{3}}$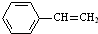 +H2,下列说法正确的是( )
+H2,下列说法正确的是( )| A. | 该反应的类型为消去反应 | |
| B. | 乙苯的同分异构体共有三种 | |
| C. | 可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数均为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素都是非金属元素 | B. | M、N投入水中所得溶液中溶质相同 | ||
| C. | 三种化合物都是共价化合物 | D. | Z是地壳中含量最多的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;②当转移2mol电子时,可得到还原产物58.5g.
;②当转移2mol电子时,可得到还原产物58.5g.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
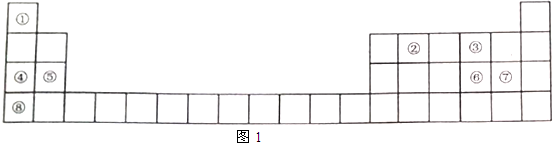

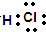 ,其中所含化学键的类型是共价键.
,其中所含化学键的类型是共价键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com