
【题目】在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)![]()
![]() mol/(L·min)
mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<![]() mol/(L·min)
mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是放热反应的是( )
A.铝片与稀H2SO4反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与CO2反应
D.NaOH与HCl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+O2(g)=2H2O(l) ΔH=-569.6kJ/mol,2H2O(g)=2H2(g)+O2(g) ΔH=+482.1 kJ/mol。现有1g液态H2O,蒸发时吸收的热量是 ( )
A. 2.43 kJ B. 4.86 kJ C. 43.8 kJ D. 87.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[有机化学基础]
龙癸醛是一种珍贵香料,广泛应用于香料、医药、染料及农药等行业。其合成路线如图所示(部分反应产物和反应条件已略去)

回答下列问题
(1)下列有关R和烯烃C3H6的说法不正确的是_________。(填代号)
A.它们的碳原子均在同一平面 B.它们都能使酸性KMnO4溶液褪色
C.它们都能发生加成反应 D.它们都含有碳碳双键
(2)反应②的类型是____________,反应③的类型是__________。
(3)T所含官能团的名称是___________;反应⑥的化学方程式为________。
(4)X的实验式为_____________。
(5)遇氯化铁溶液发生显色反应的T的同分异构体有_______种,其中,在核磁共振氢谱上有4组峰且峰面积比为1:2:3:6的结构简式为________________。
(6)参照上述流程图,以2一甲基-1,3-丁二烯为原料,经三步制备2一甲基-1,4一丁二醛的合成路线:

反应条件1所选用的试剂为_________,反应条件2所选用的试剂及条件为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃,体积固定的密闭容器中,发生反应A(g)+3B(g)![]() 2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
A. 正向移动 B. 逆向移动
C. 不移动 D. 再次达新平衡时,C的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+ Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 该温度下此反应的平衡常数K = 1.44
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 反应前2 min的平均速率v(Z) = 2.0×10-3 mol/(L·min)
D. 其他条件不变,再充入0.2 mol X,平衡时Y的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,保持一定温度,在一定条件下进行如下反应A(g)+2B(g)![]() 3C(g),已知起始时加入2 mol A(g)和3 mol B(g),达平衡后,生成a mol C(g)。此时,C(g)在反应混合气体中的体积分数为_____________(用含字母a的代数式表示)。
3C(g),已知起始时加入2 mol A(g)和3 mol B(g),达平衡后,生成a mol C(g)。此时,C(g)在反应混合气体中的体积分数为_____________(用含字母a的代数式表示)。
(1)相同实验条件下,若在同一容器中改为开始加入1 mol A和1.5mol B,达平衡时C的物质的量为________mol(用含字母a的代数式表示)。此时C在反应混合物中的体积分数_____________(填“增大”、“减小”或“不变”)。
(2)相同实验条件下,若在同一容器中改为开始时加入2 mol A和2 mol B,达平衡时,要求C在混合物中体积分数与(1)相同,则开始时还需加入_________mol C,平衡时C的物质的量为_______________mol(用含字母a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中ffi重要试剂,可由NO与Cl2在常温常压(或稍低温度)下合成,其熔点-64.5℃,沸点-5.5℃,遇水易水解。实验室模拟制备装置如图所示(部分夹持装置省略),D中三颈烧瓶置于-10℃冰盐水中。

经查阅资料:NO与NaOH溶液不反应,但NO2+NO+2NaOH =2NaNO2+H2O
(1)仪器甲的名称是________。
(2)图示装置中恒压漏斗与分液漏斗相比,其优点为___________。
(3) NOC1分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________。
(4)实验开始时,先打开K1、K2,关闭K3,打开分液漏斗活塞滴入适量稀硝酸,至C中红棕色完全消失后,关闭K1、K2,此时装置C的作用为___________。滴入适量浓盐酸,点燃酒精灯,当_______(填装置符号)中充满黄绿色气体时,打开K1、K3,制备NOC1。
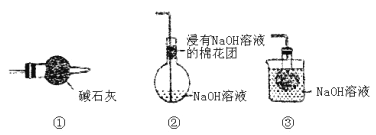
(5)装置乙中装有无水CaCl2,其作用为_______;丙为尾气处理装置,则最佳选择为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com