
【题目】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都具有10个电子,其结构特点如下:
粒子代码 | a | b | c | d | e | f | g |
原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c和f在一定条件下形成一个g分子和一个d分子,试写出:
(1)a粒子的原子结构示意图___________
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为___>_____ (用化学式表示)。
(3)d与一种含有极性键双核18电子分子反应的化学方程式为 ______。
(4)g与一种含有非极性键双核18电子分子反应的化学方程式为__________
上述反应中,断裂化学键是__________,写出的化学键是________(填“离子键”、“极性键”、“非极性键”、“氢键”)
【答案】 ![]() NaOH Mg(OH)2 NH3+HCl=NH4Cl 2H2O+2F2=4HF+O2 极性键和非极性键 极性键和非极性键
NaOH Mg(OH)2 NH3+HCl=NH4Cl 2H2O+2F2=4HF+O2 极性键和非极性键 极性键和非极性键
【解析】本题考查元素周期表和元素周期律的应用,通过10电子的微粒进行判断,a是单核,且不带电荷,即a为Ne,b为单核,且带有一个单位正电荷,推出b为Na+,c为双核,带有一个单位负电荷,即c为OH-,d是多核,不带电荷,由极性键构成的四原子分子,则d为NH3,e为单核,带有2个单位正电荷,即e为Mg2+,f是多核,带有一个单位正电荷,即f为H3O+或NH4+,g是多核,不带电荷,g可能是H2O,也可能是CH4,c和f在一定条件下形成一个g分子和NH3,说明NH4++OH-![]() NH3↑+H2O,推出f为NH4+,g为H2O,(1)Ne是10号元素,原子结构示意图为
NH3↑+H2O,推出f为NH4+,g为H2O,(1)Ne是10号元素,原子结构示意图为![]() ;(2)b和e相应元素的最高正价氧化物对应水化物是NaOH和Mg(OH)2,Na的金属性强于Mg,则NaOH的碱性强于Mg(OH)2;(3)d为NH3,极性键的18电子分子为HCl,反应方程式为NH3+HCl=NH4Cl;(4)含有非极性键的双核18电子分子,此分子是F2,方程式为2F2+2H2O=4HF+O2;F2中F-F是非极性键,断裂,H2O中H-O键断裂,是极性键,生成HF,生成极性键,还生成O2,生成非极性键。
;(2)b和e相应元素的最高正价氧化物对应水化物是NaOH和Mg(OH)2,Na的金属性强于Mg,则NaOH的碱性强于Mg(OH)2;(3)d为NH3,极性键的18电子分子为HCl,反应方程式为NH3+HCl=NH4Cl;(4)含有非极性键的双核18电子分子,此分子是F2,方程式为2F2+2H2O=4HF+O2;F2中F-F是非极性键,断裂,H2O中H-O键断裂,是极性键,生成HF,生成极性键,还生成O2,生成非极性键。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如下图所示:

(1)则25℃时水的电离平衡曲线应为_________(填“A”或“B”),请说明理由 。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为__________.
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_________________.
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5.请分析其原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在常温下发生水解时,对应的离子方程式正确的是( )
①Na2CO3:CO32-+2H2O![]() H2O+CO2↑+2OH-
H2O+CO2↑+2OH-
②NH4Cl:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
③CuSO4:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
④NaF:F-+H2O![]() HF+OH-
HF+OH-
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A. 温度一定时,Ksp(SrSO4)随c(SO42—)的增大而减小
B. 三个不同温度中,313 K时Ksp(SrSO4)最大
C. 283 K时,图中a点对应的溶液是饱和溶液
D. 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是
A.容量瓶中原有少量的蒸馏水
B.移液时,不慎将液体流到瓶外
C.容量瓶盛过KOH溶液,使用前未洗涤
D.定容时仰视刻度线和液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
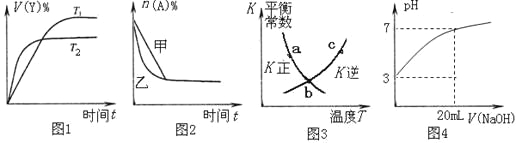
A. 图1表示可逆反应“2X(g)![]() Y(g)△H<0”温度T1<T2的情形
Y(g)△H<0”温度T1<T2的情形
B. 图2表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C. 图3中a、b、c三点中只有b点已经达到化学平衡状态
D. 图4是向20 mL pH =3的醋酸溶液中滴加pH=11的NaOH溶液过程中pH变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯元素的说法正确的是( )
A. HCl具有很强的酸性,且只有氧化性没有还原性
B. ![]() 、
、![]() 为不同的核素,有完全不同的化学性质
为不同的核素,有完全不同的化学性质
C. 1.12L含有1 .7NA个质子(NA表示阿伏加德罗常数)
D. 氯气可从KI溶液中置换出I2,说明氯的非金属性比碘强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.稀硫酸滴在铁片上:Fe+2H+=Fe3++H2↑
B.硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
C.足量盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O
D.氢氧化铜与稀硫酸混合:H++OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同位素常用做环境分析指示物,下列对同位素的说法正确的是( )
A.34S原子核内的中子数为16
B.13C和15N原子核内的质子数相差2
C.16O与18O的核电荷数相等
D.2H+质量与1H+的质量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com