
下列说法正确的是( )
A.在钠、钾、铷,三种单质中,铷的熔点最高
B.充电电池的化学反应原理是氧化还原反应,充电是使放电时的氧化还原反应逆向进行,燃料电池的能量利用率可达100%
C.化学键可以使离子相结合,也可以使原子相结合
D.氟利昂-12(CF2Cl2)有两种同分异构体
科目:高中化学 来源: 题型:
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )
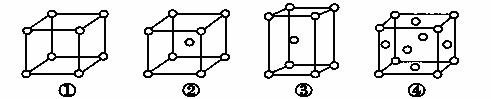
A.①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积
B.晶胞中原子的配位数分别为:①6, ②8 ,③8, ④12
C.金属镁采取③的堆积方式
D.空间利用率的大小关系为:① < ② < ③ < ④
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为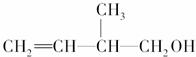 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
A.能与金属钠发生反应并放出氢气B.能在催化剂作用下与H2发生加成反应
C.能发生银镜反应D.在浓H2SO4催化下能与乙酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
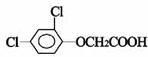
A.该物质的分子式为C8H6Cl2O3
B.1mol该物质与氢氧化钠反应消耗氢氧化钠5mol
C.可发生加成反应和取代反应
D.1mol该物质与钠反应可产生氢气11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有三个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol, I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)Y在周期表中的位置 ,Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(2)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ键。
(3)写出X与NaOH溶液反应的离子方程式 。超高导热绝缘耐高温纳米XW在绝缘材料中应用广泛,晶体与金刚石类似,属于 晶体.W的最简单氢化物容易液化,理由是 。
(4)Z的基态原子核外电子排布式为 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示错误的是
A.氧化剂是O2 B.HO2在碱中不能稳定存在
C.氧化产物是HO2 D.1 molZ参加反应有1 mol电子发生转移
(5)已知Z的晶胞结构如下图所示,又知Z的密度为9.00 g·cm-3,则晶胞边长为 ;ZYO4常作电镀液,其中YO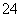 的空间构型是 ,其中Y原子的杂化轨道类型是 。
的空间构型是 ,其中Y原子的杂化轨道类型是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
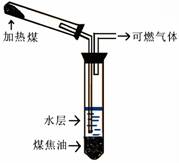
煤的干馏实验如图所示:
(一)水层中溶有铵盐、氨,可以作为化工原料
(1)下列方法中,不能用于实验室制取氨的是( )
A.在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
B.加热试管中的氯化铵固体
C.将烧瓶中的浓氨水加热
D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
(二)可燃气体被称为焦炉气,含有甲烷、乙烯、CO、氢气。
(2)检验焦炉气中是否含有乙烯应加入的化学试剂 ;
(3)CO有毒,汽车尾气中也含有CO,同时含有的NO也是一种污染物,汽车燃料中不含氮元素,那么NO是如何产生的?请用化学方程式说明 。
治理汽车尾气中CO、NO的一种方法是:在排气管安装催化转化装置,使NO、CO反应生成无污染的气体,化学方程式为 。
(三)煤焦油中有苯、甲苯、二甲苯、酚类
(4)酚类和醇类的官能团都是羟基,常见的醇类物质为乙醇,向盛有乙醇的烧杯里投入一小块金属钠,可以观察到的现象是( )
A.钠块沉在乙醇液面以下 B.钠块熔成小球
C.钠块在乙醇液面上游动 D.钠块表面有气泡产生
(四)干馏剩余的固体物质主要是焦炭,可以用于冶金、合成氨造气、电石、燃料。
(5)例如:以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
①在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体;
②在稀有气体(如Ar)氛围和加热条件下,用Mg与TiCl4反应可以得到的钛。写出两步的方程式。
。 。
(五)煤的干馏需要隔绝空气加强热,而实验室中用于灼烧或熔融固体物质的常用仪器是坩埚,其材质种类很多,实验时应根据物质的性质加以选择。熔融烧碱时,不能使用普通的玻璃坩埚、石英坩埚和陶瓷坩埚,可以使用 (填材料名称)坩埚。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在指定溶液中能大量共存的是 ( )
A.1.0 mol·L-1的KNO3溶液:H+、Fe 2+、Cl-、SO
2+、Cl-、SO
B.1.0 mol·L-1的FeCl2溶液:NO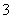 、Na+、K+、ClO-
、Na+、K+、ClO-
C.使酚酞变红的溶液中:Na+、Cl-、SO 、Fe3+
、Fe3+
D.酸性溶液中:NO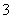 、SO
、SO 、Fe3+、Mg2+
、Fe3+、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中有关物质的量浓度关系和计算不正确的是:
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.已知25°C时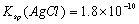 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到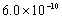 mol·L-1
mol·L-1
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有C(HA-) >C(H+)>C(A2-)>C(H2A)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com